Содержание
- 2. Энергия Гиббса реакции в нестандартных условиях Сi ≠ С0 ΔrGi =ΔrG0i + R⋅T⋅lnCi ΔrG = (νc⋅ΔfG0C+
- 3. 4.7 Равновесие – термодинамические условия (ΔrG = 0) [Равновесные концентрации (Ci )pvi постоянны]
- 4. Сдвиг равновесия. Определение направления сдвига. Правило Ле Шателье Равновесие νаA + νbB ↔ νсC + νdD
- 5. Константа равновесия К, её размерность. Связь между К [кинетич.К-f(T), K≠f(C)] и стандартной К0 [термодинам.К0–f(T, т/д функций)]
- 6. Равновесие – динамическое (непрерывное протекание прямой и обратной реакции в состоянии равновесия) реакция νаA + νbB
- 7. Расчет равновесного состава(концентраций) газовой смеси Расчет К0(Т) термодинамической Для определенной Т рассчитывают → ΔrG0(T)=ΔrH0(T) –Т·ΔrS0(T). Затем
- 8. Пример. Диссоциация АВ при Р -const и температуре Т АВ = А + В ni САВ-z
- 9. Равновесие в растворах (дисперсных системах)
- 10. Электролитическая диссоциация С0 - общая концентрация СД - конц.молекул в виде ионов Сильн.: α → 1
- 11. Ионное произведение воды H2O ⇔ H+ + OH- Нейтральная среда [H+] = [OH–] = 10-7 [моль/л]
- 12. Водородный показатель pH = –lg[H+] Нейтральная среда pH = 7 Кислая среда pH Щелочная среда pH
- 13. Растворы кислот и оснований МеOH ⇔ Ме+ + OH- Слабые электролиты α → 0 Сильные электролиты
- 14. Многоосновные кислоты и основания H2An ⇔ H+ + НAn- HAn- ⇔ H+ + An2- Ка1 >>
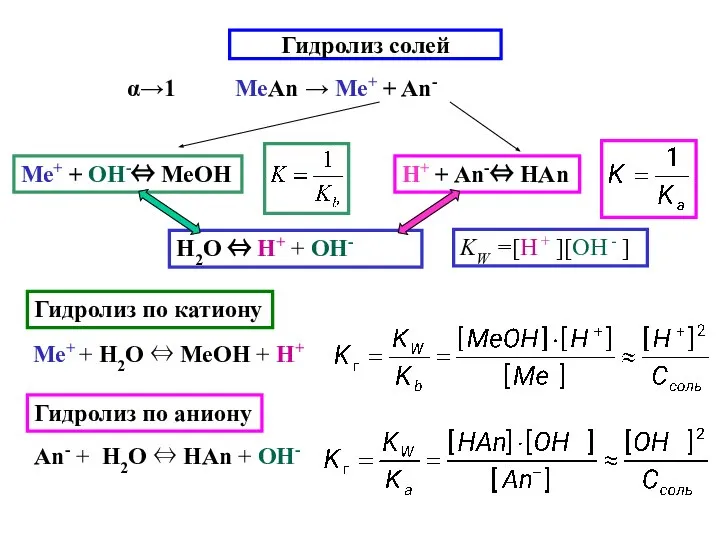
- 15. Гидролиз солей α→1 МеAn → Ме+ + An- Гидролиз по катиону Гидролиз по аниону
- 16. Примеры гидролиза солей 1) Kb→0; Ka→ ∞ CuSO4 → Cu2+ + SO42- 2 CuSO4+ 2 H2O
- 17. Произведение растворимости - ПР S-растворимость осадка[моль/л] [Kat+] = x·S [моль/л]
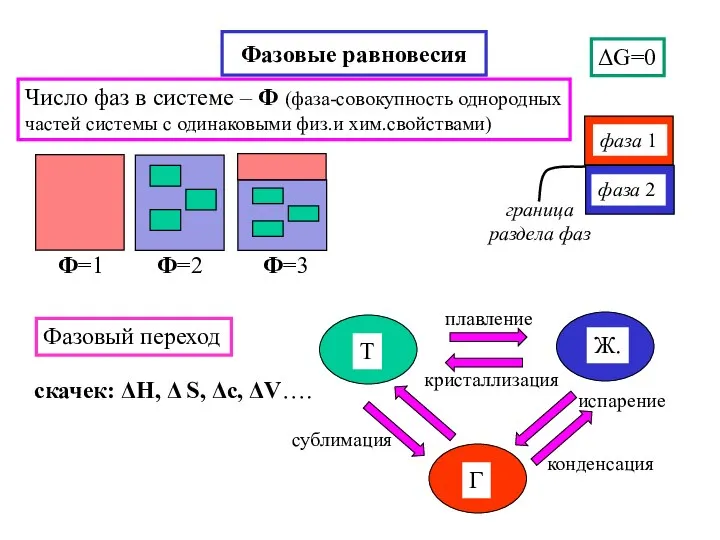
- 18. Фазовые равновесия ΔG=0 Фазовый переход скачек: ΔH, Δ S, Δc, ΔV…. Число фаз в системе –
- 19. Число компонентов – К (независимые составные части системы) Число видов молекул, необходимое и достаточное для образования
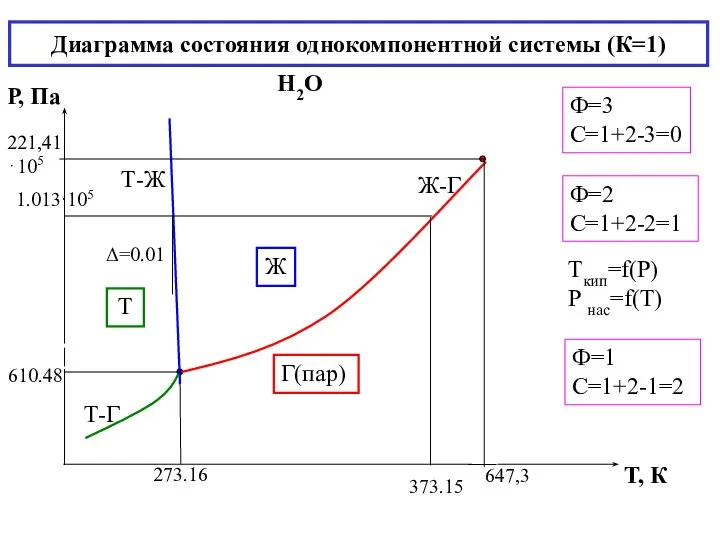
- 20. Диаграмма состояния однокомпонентной системы (К=1) Н2О Ф=2 С=1+2-2=1 Ф=3 С=1+2-3=0 Ф=1 С=1+2-1=2 Ж Г(пар) Т Tкип=f(Р)
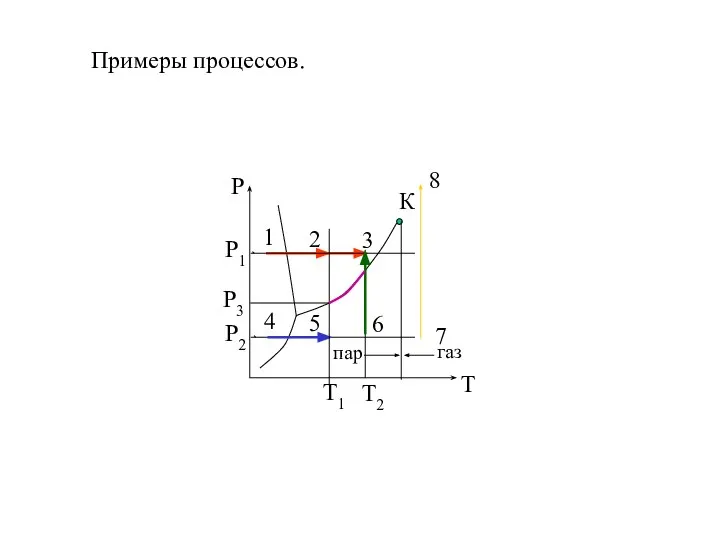
- 21. Примеры процессов.
- 22. Двухкомпонентная система [К=2(вода+ растворенное вeщество А)], молекулярный раствор. α→ 0 p0 –давление насыщенного пара (Н2Опар )
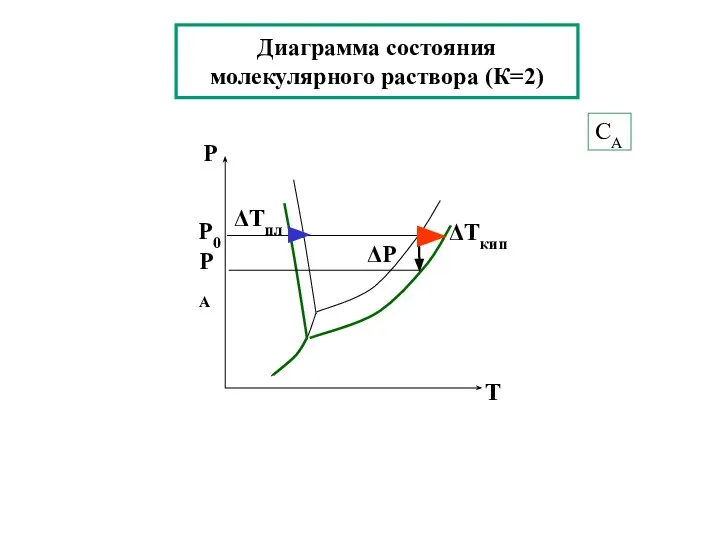
- 23. Диаграмма состояния молекулярного раствора (К=2) СА ΔP
- 24. Кипение и кристаллизация растворов Повышение температуры кипения раствора по сравнению с чистым растворителем (ΔТкип) прямо пропорционально
- 25. Эбуллиоскопические и криоскопические постоянные некоторых растворителей
- 27. Скачать презентацию

![4.7 Равновесие – термодинамические условия (ΔrG = 0) [Равновесные концентрации (Ci )pvi постоянны]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1358975/slide-2.jpg)

![Константа равновесия К, её размерность. Связь между К [кинетич.К-f(T), K≠f(C)] и](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1358975/slide-4.jpg)





![Ионное произведение воды H2O ⇔ H+ + OH- Нейтральная среда [H+]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1358975/slide-10.jpg)
![Водородный показатель pH = –lg[H+] Нейтральная среда pH = 7 Кислая](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1358975/slide-11.jpg)



![Произведение растворимости - ПР S-растворимость осадка[моль/л] [Kat+] = x·S [моль/л]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1358975/slide-16.jpg)

![Двухкомпонентная система [К=2(вода+ растворенное вeщество А)], молекулярный раствор. α→ 0 p0](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1358975/slide-21.jpg)


 Полимеры. Классификация полимеров
Полимеры. Классификация полимеров Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Подготовка учащихся к практическим турам олимпиад по химии
Подготовка учащихся к практическим турам олимпиад по химии Мягкие лекарственные формы. Мази, капсулы, суппозитории, пластыри
Мягкие лекарственные формы. Мази, капсулы, суппозитории, пластыри Органічні речовини як основа сучасних матеріалів. Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна
Органічні речовини як основа сучасних матеріалів. Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна Выполнил: ученики 9 класса Проверил: учитель химии Санеева Л.П.
Выполнил: ученики 9 класса Проверил: учитель химии Санеева Л.П. Водород. Растворы. 8 класс
Водород. Растворы. 8 класс Оптическая литография
Оптическая литография Поняття про хімічні засоби захисту рослин (11 клас)
Поняття про хімічні засоби захисту рослин (11 клас) Предмет органической химии. Тест 18
Предмет органической химии. Тест 18 Материалы космической техники
Материалы космической техники Химические элементы O2 и N2
Химические элементы O2 и N2 Загальні способи добування солей. Класифікація неорганічних речовин
Загальні способи добування солей. Класифікація неорганічних речовин Презентация по Химии "Соединения алюминия" - скачать смотреть бесплатно
Презентация по Химии "Соединения алюминия" - скачать смотреть бесплатно Описание основных типов магматических горных пород
Описание основных типов магматических горных пород Смог и его виды
Смог и его виды Природні сполуки алюмінію і методи одержання
Природні сполуки алюмінію і методи одержання Каталитический риформинг
Каталитический риформинг Химия и пища
Химия и пища Дисперсные системы. Поверхностная энергия
Дисперсные системы. Поверхностная энергия Электрохимические методы анализа
Электрохимические методы анализа Chemical kinetics
Chemical kinetics Ядро атома (тест)
Ядро атома (тест) Эндогенная серия. Вулканогенно-осадочная группа
Эндогенная серия. Вулканогенно-осадочная группа Углеводороды. Алканы
Углеводороды. Алканы Процессы дыхания, брожения, обмена веществ, фотосинтеза, нервная деятельность
Процессы дыхания, брожения, обмена веществ, фотосинтеза, нервная деятельность Псевдогалогены и их соединения
Псевдогалогены и их соединения Массообменные процессы
Массообменные процессы