Содержание
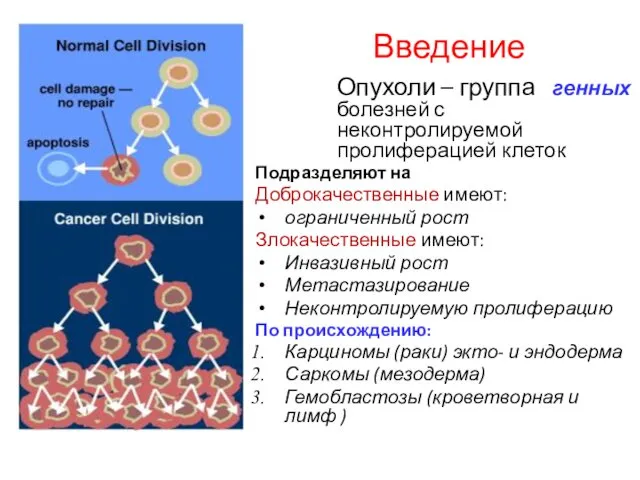
- 2. Введение Опухоли – группа генных болезней с неконтролируемой пролиферацией клеток Подразделяют на Доброкачественные имеют: ограниченный рост
- 3. Этиология опухолей В 80% возникновение опухолей связано с воздействием факторов внешней среды (образ жизни, питание, вредные
- 4. Радиационный канцерогенез Интенсивное УФО, проживание на территориях, зараженных радионуклидами, увеличивает риск появления меланом и карцином кожи,
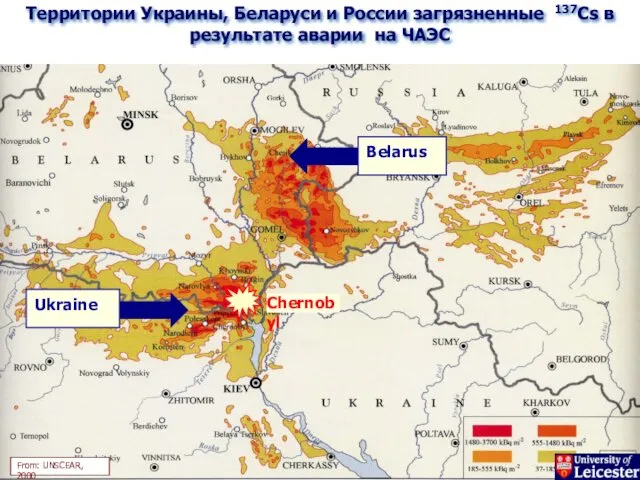
- 5. Территории Украины, Беларуси и России загрязненные 137Cs в результате аварии на ЧАЭС From: UNSCEAR, 2000 Chernobyl
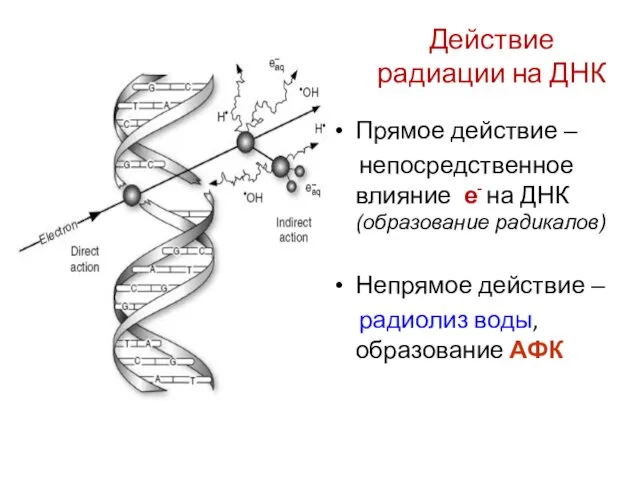
- 6. Действие радиации на ДНК Прямое действие – непосредственное влияние е- на ДНК (образование радикалов) Непрямое действие
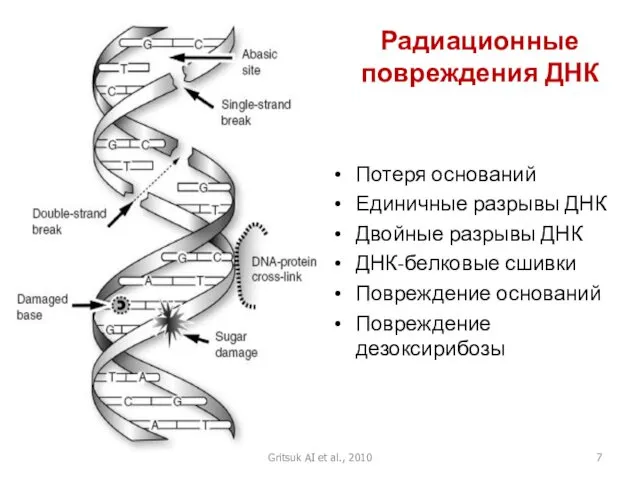
- 7. Радиационные повреждения ДНК Потеря оснований Единичные разрывы ДНК Двойные разрывы ДНК ДНК-белковые сшивки Повреждение оснований Повреждение
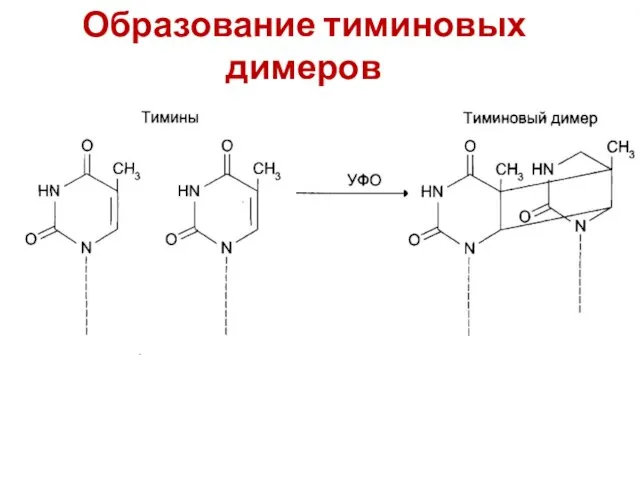
- 8. Образование тиминовых димеров
- 9. Механизм образования АФК О2 + е- ? О2˙+ е- ? Н2О2 Источники е- - ионизирующее излучение
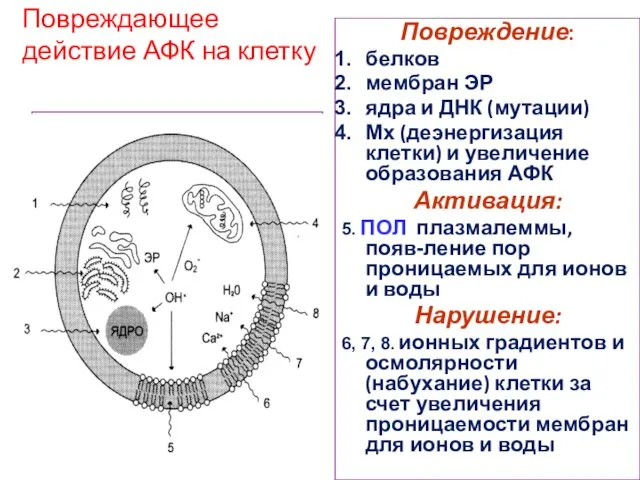
- 10. Повреждающее действие АФК на клетку Повреждение: белков мембран ЭР ядра и ДНК (мутации) Мх (деэнергизация клетки)
- 11. Антиоксидантная защита (АОЗ) Неферментативная – АО вещества образующие менее активные радикалы и «гасят» цепные реакции (вит
- 12. Химический канцерогенез Большинство канцерогенов существует в форме проканцерогенов, которые в печени превращ в активные формы, реагирующими
- 13. Основные химические канцерогены (ХК) Все ХК (орг. и неорг.), обычно электрофилы, реагируют с нуклеофильными группами ДНК
- 14. Химические канцерогены (ХК) ПАУ- продукты неполного сгорания угля,нефти, табака, пиролиза масел, органических компонентов пищи и др.
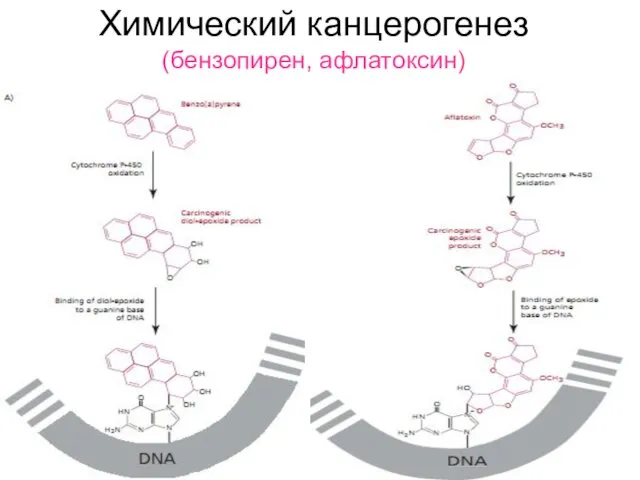
- 15. Химический канцерогенез (бензопирен, афлатоксин)
- 16. Химические канцерогены (прод.) Ароматические амины - анилиновые красители и в-ва используемые в резиновой пром-сти Нитрозамины –
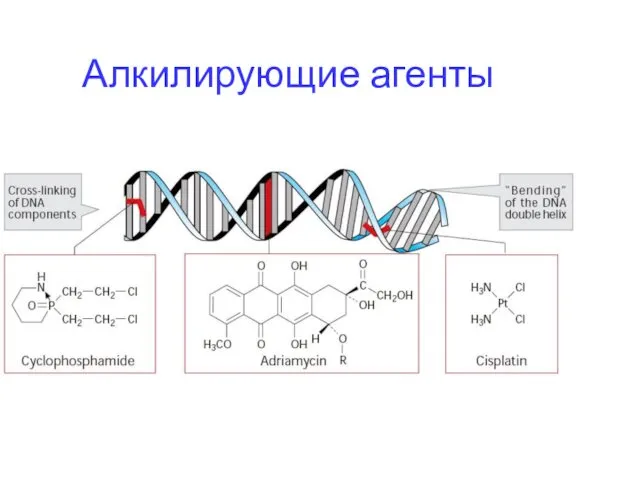
- 17. Алкилирующие агенты
- 18. Вирусный канцерогенез ДНК-содержащие вирусы (герпеса, аденовирус, ветряной оспы) полностью или частично встраиваются в геном хозяина и
- 19. Наследственная предрасположенность Нестабильность генома приводит в дефектам системы репарации ДНК У детей предрасположенность к Rb (ретино-бластоме)
- 20. Нестабильность генома – эпигенетический феномен Нестабильность генома вызвана длительными изменениями экспрессии генов и переносится через много
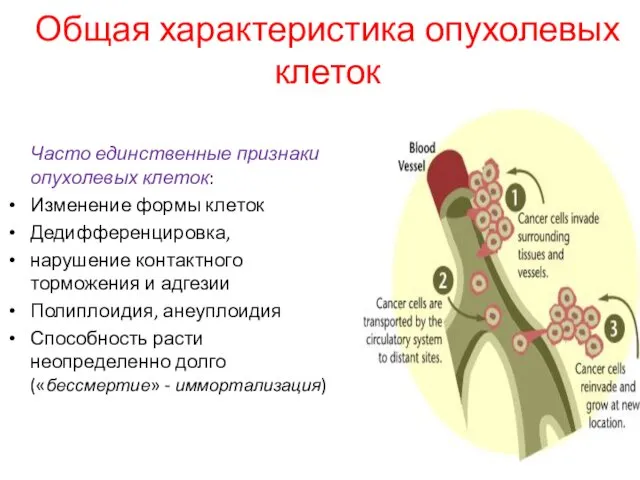
- 21. Общая характеристика опухолевых клеток Часто единственные признаки опухолевых клеток: Изменение формы клеток Дедифференцировка, нарушение контактного торможения
- 22. Защитные механизмы опухолевых клеток Высокий уровень экспрессии шаперона БТШ 70 (Hsp70 ), который: фолдирует новые белки
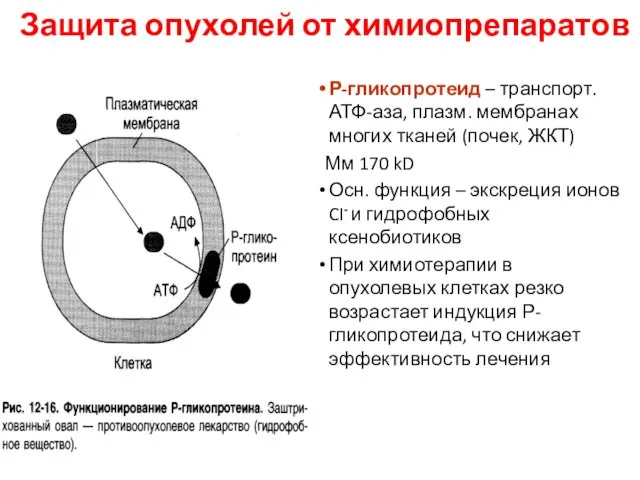
- 23. Защита опухолей от химиопрепаратов Р-гликопротеид – транспорт. АТФ-аза, плазм. мембранах многих тканей (почек, ЖКТ) Мм 170
- 24. Особенности метаболизма опухоли подчинены обеспечению роста клеток ↑ активность рибонуклеотидредуктазы (рибоза —> дезоксирибоза) и синтеза ДНК
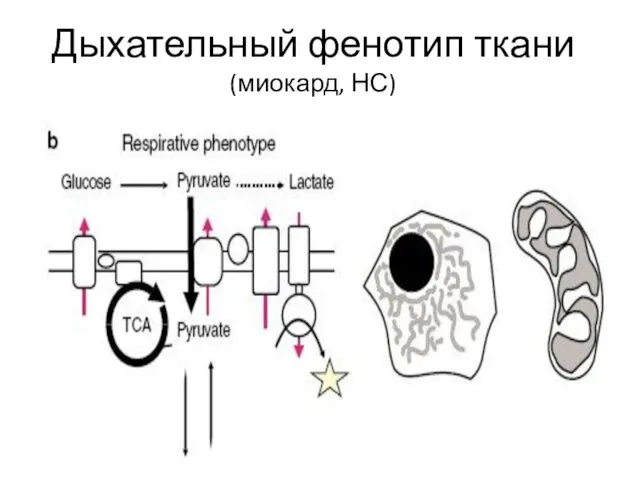
- 25. Дыхательный фенотип ткани (миокард, НС)
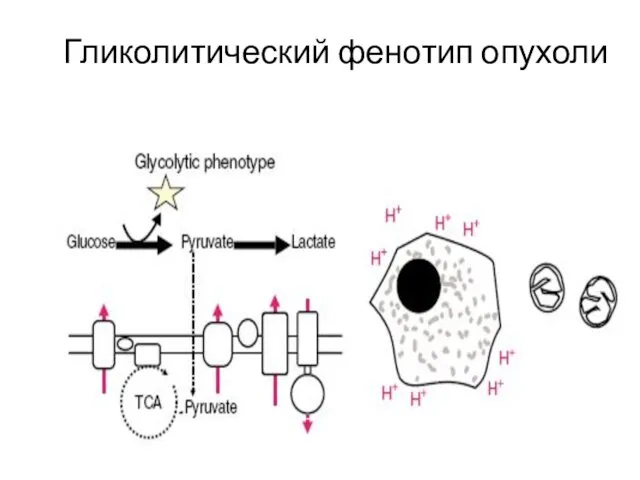
- 26. Гликолитический фенотип опухоли
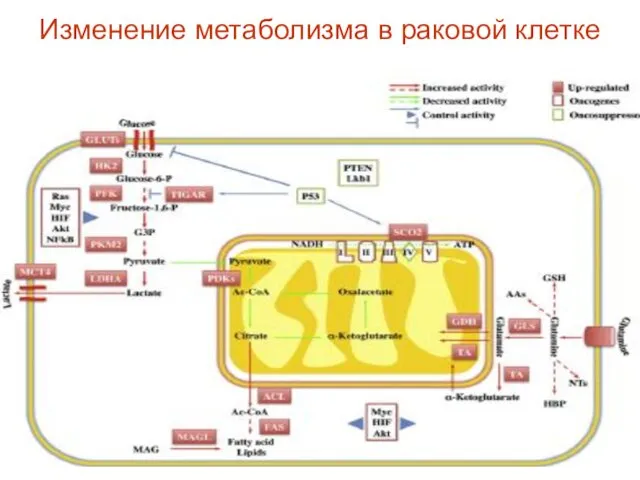
- 27. Изменение метаболизма в раковой клетке
- 28. Особенности метаболизма опухоли (прод) В связи с этим опухоль: Является ловушкой глюкозы, АК, ЖК, АО и
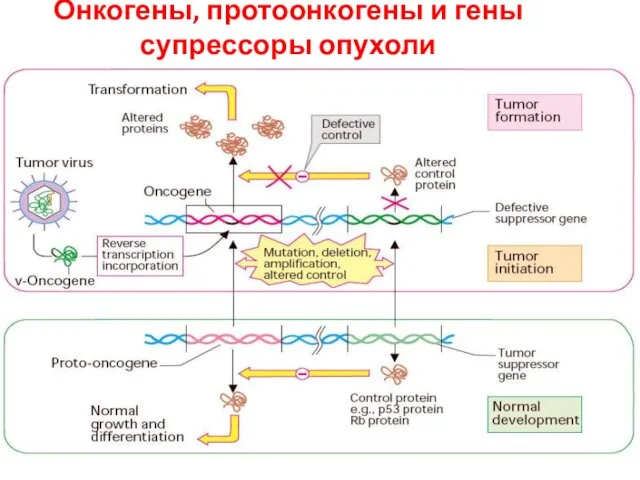
- 29. Онкогены, протоонкогены и гены супрессоры опухоли Протонкогены – гены экспрессирующие белки контролирующие рост ФР, их рецепторы,
- 30. Онкогены, протоонкогены и гены супрессоры опухоли
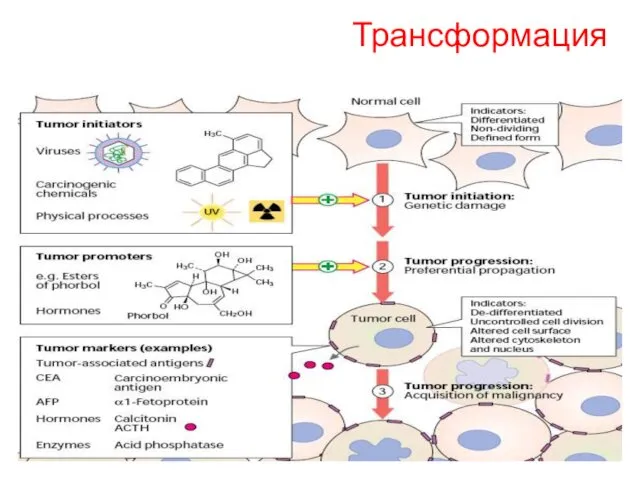
- 31. Трансформация
- 32. Механизмы трансформации 1. нарушение баланса генома «Выключение» генов путем метилирования ДНК Превращение протоонкогенов в онкогены Точечные
- 33. Основные подходы лабораторной диагностики опухолей Опухолевые маркеры Онкофетальные белки (а-ФП, РЭА и др.) мРНК онкофетальных белков
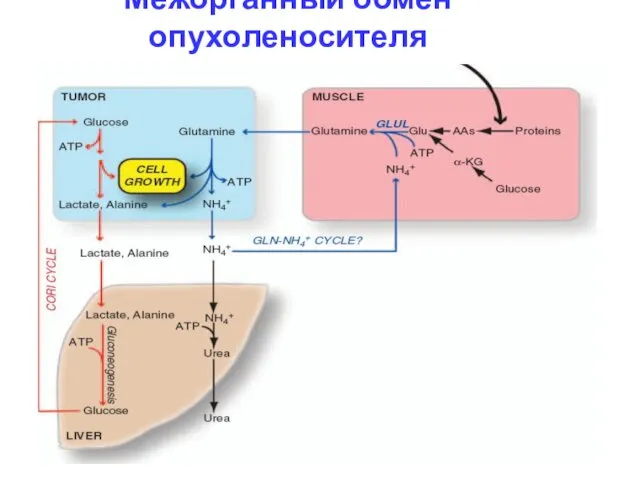
- 34. Межорганный метаболизм кахектичного ракового пациента Рост опухоли сопровождается потреблением глюкозы и глн с секрецией лактата, ала
- 35. Межорганный обмен опухоленосителя
- 36. мРНК теломеразы Теломераза синтезирует концевые участки хромосом (теломер) Обнаружена во всех c-r клетках мРНК теломеразы присутствует
- 37. Метилированная ДНК - ценный биомаркер диагностики рака 1. Ряд генов, вовлеченных в канцерогенез, инактивируется путем метилирования
- 39. Скачать презентацию




















 Закономерности развития звукопроизношения в онтогенезе
Закономерности развития звукопроизношения в онтогенезе Лечебное питание
Лечебное питание Ішек иерсиниозы
Ішек иерсиниозы Тазовое предлежание плода, классификация, актуальность
Тазовое предлежание плода, классификация, актуальность Пептиды. Применение в косметологии
Пептиды. Применение в косметологии Алгоритм диагностики и оказания скорой помощи при угрожающих жизни поражениях сердечно-сосудистой системы
Алгоритм диагностики и оказания скорой помощи при угрожающих жизни поражениях сердечно-сосудистой системы Слайд-лекция №14. Лекарственные средства влияющие на функции органов пищеварения
Слайд-лекция №14. Лекарственные средства влияющие на функции органов пищеварения Algorithm of diagnostics and first aid at eclampsia
Algorithm of diagnostics and first aid at eclampsia Иммунитет в защите и повреждении организма. (Лекция 6)
Иммунитет в защите и повреждении организма. (Лекция 6) МРТ – диагностика патологии позвоночника. УЗИ – диагностика патологии коленного сустава
МРТ – диагностика патологии позвоночника. УЗИ – диагностика патологии коленного сустава Методика самообследования молочных желёз
Методика самообследования молочных желёз Донорство крови
Донорство крови Пикфлоуметрия
Пикфлоуметрия ГРВІ, грип, парагрип
ГРВІ, грип, парагрип Лечебно-оздоровительный туризм Беларуси
Лечебно-оздоровительный туризм Беларуси Информация для публикации: как её добыть
Информация для публикации: как её добыть Особенности становления речи у детей близнецов
Особенности становления речи у детей близнецов Дизентерия (шигеллёз)
Дизентерия (шигеллёз) Познание людей в профессиональной и обыденной жизни по физиогномическим признакам. Характеристика рта, носа, ушей
Познание людей в профессиональной и обыденной жизни по физиогномическим признакам. Характеристика рта, носа, ушей Организация питания в детском саду
Организация питания в детском саду Экзамены. Умей владеть собой
Экзамены. Умей владеть собой Хадмат Гавсуддин 421 леч исправл
Хадмат Гавсуддин 421 леч исправл Бактериальный посев мокроты
Бактериальный посев мокроты Что такое гепатит В?
Что такое гепатит В? Сибирская язва. Сибиреязвенные бациллы (род Bacillus)
Сибирская язва. Сибиреязвенные бациллы (род Bacillus) Хронофармакология. Хронобиология и хрономедицина
Хронофармакология. Хронобиология и хрономедицина Выделение. Гомеостаз
Выделение. Гомеостаз Чума 21 века
Чума 21 века