Содержание
- 2. MỤC LỤC
- 3. 1.GIỚI THIỆU
- 4. 1.GIỚI THIỆU Công nghệ y tế có thể được coi như bất kỳ công nghệ được
- 5. 2.ĐÁNH GIÁ CÔNG NGHỆ Y TẾ [1] World Health Organization , Health technology assessment of medical
- 6. 2.1 ĐÁNH GIÁ CNYT CHO QUYẾT ĐỊNH DỰA TRÊN BẰNG CHỨNG Người cung cấp dữ liệu
- 7. 2.2 ĐÁNH GIÁ CNYT TRONG HỆ THỐNG Y TẾ Ra quyết định và quản trị ĐCNYT
- 8. 2.3 HỢP TÁC QUỐC TẾ TRONG ĐGCNYT [1] World Health Organization , Health technology assessment of
- 9. 2.4 KHÓ KHĂN CỦA CÁC NƯỚC ĐANG PHÁT TRIỂN TRONG ĐGCNYT Tiết kiệm chi phí để
- 10. 3. QUẢN LÍ CÔNG NGHỆ Y TẾ "Xây dựng cho phù hợp chiến lược và kế
- 11. 3.1 QUY ĐỊNH ĐỔI MỚI VỀ THIẾT BỊ Y TẾ 1938: thiết bị y tế lần
- 12. 3.2 BỐN QUY TẮC TIẾP THỊ THIẾT BỊ Y TẾ Ở THỊ TRƯỜNG MỸ 1 2
- 13. 3.3 VẤN ĐỀ ĐẠO ĐỨC TRONG NHỮNG NGHIÊN CỨU KHẢ THI Trong một nghiên cứu tính
- 14. 3.4 Y ĐỨC TRONG TRƯỜNG HỢP CẤP CỨU Tổ chức sức khỏe đã cho phép sử
- 15. 3.5 VẤN ĐỀ ĐẠO ĐỨC TRONG SỬ DỤNG ĐIỀU TRỊ Thứ hai Tóm lại Vì các
- 16. 4.SO SÁNH ĐÁNH GIÁ VÀ QUẢN LÍ CNYT [1] World Health Organization , Health technology assessment
- 17. 5.TÀI LIỆU THAM KHẢO [1] World Health Organization , Health technology assessment of medical devives, Switzerland,
- 19. Скачать презентацию
MỤC LỤC
MỤC LỤC
1.GIỚI THIỆU
1.GIỚI THIỆU
1.GIỚI THIỆU
Công nghệ y tế có thể được coi như
1.GIỚI THIỆU
Công nghệ y tế có thể được coi như
Quản lí và đánh giá công nghệ y tế là những chức năng bổ sung cho nhau để đảm bảo sự giới thiệu thích hợp và chức năng của thiết bị y tế.
Những người từ lĩnh vực đánh giá và quản lí thiết bị y tế từng có ít sự tương tác lẫn nhau trong quá khứ
Quản lí và đánh giá thiết bị y tế đều là những yế tố quan trọng trong sự thành công của chính sách công nghệ y tế quốc gia
[1] World Health Organization , Health technology assessment of medical devives, Switzerland, 2011
2.ĐÁNH GIÁ CÔNG NGHỆ Y TẾ
[1] World Health Organization , Health
2.ĐÁNH GIÁ CÔNG NGHỆ Y TẾ
[1] World Health Organization , Health
2.1 ĐÁNH GIÁ CNYT CHO QUYẾT ĐỊNH DỰA TRÊN BẰNG CHỨNG
Người
2.1 ĐÁNH GIÁ CNYT CHO QUYẾT ĐỊNH DỰA TRÊN BẰNG CHỨNG
Người
Người sử dụng dữ liệu
( những nhà hoạch định chính sách).
Sự chặt chẽ về kĩ thuật của các bằng chứng mà dựa trên nó để đưa ra quyết định nhận được sự quan tâm ngày càng tăng
[1] World Health Organization , Health technology assessment of medical devives, Switzerland, 2011
2.2 ĐÁNH GIÁ CNYT TRONG HỆ THỐNG Y TẾ
Ra quyết định
2.2 ĐÁNH GIÁ CNYT TRONG HỆ THỐNG Y TẾ
Ra quyết định
ĐCNYT hỗ trợ ra quyết định minh bạch , và do đó tham gia từ tất cả các bên liên quan bao gồm cả dân sự xã hội
Thể chế hóa đánh giá công nghệ y tế
Hệ thống hóa các tổ chức ĐGCNYT, dựa trên ngân sách nhà nước hoặc tự chủ như các phòng nghiên cứu của bệnh viện, hay các trường đại học y tế kĩ thuật.
Đánh giá công nghệ y tế và sự đổi mới cách tân
Sự đổi mới cách tân đóng vai trò quan trọng trong tiến trình y tế và đóng góp vào sức khỏe cộng đồng. Bù lại cung cấp sự khuyến khích đổi mới, hình thành 2 chu kì phản hồi. Và nên nhớ là con người muốn sức khỏe, mà công nghệ y tế chỉ đơn giản là phương tiện để có được nó
Đánh giá công nghệ y tế là một phần của quản lí y tế tốt
Sự quản lí tốt như là một điểm có thể giúp tập trung vào hiệu suất trong sự chăm sóc sức khỏe, và đến lượt , cung cấp những hoạch định chính sách và chương trình quản lí với một cơ sở để nâng cao hiệu suất
[1] World Health Organization , Health technology assessment of medical devives, Switzerland, 2011
2.3 HỢP TÁC QUỐC TẾ TRONG ĐGCNYT
[1] World Health Organization ,
2.3 HỢP TÁC QUỐC TẾ TRONG ĐGCNYT
[1] World Health Organization ,
2.4 KHÓ KHĂN CỦA CÁC NƯỚC ĐANG PHÁT TRIỂN TRONG ĐGCNYT
Tiết
2.4 KHÓ KHĂN CỦA CÁC NƯỚC ĐANG PHÁT TRIỂN TRONG ĐGCNYT
Tiết
Các giải pháp ứng dụng cho đánh giá công nghệ y tế thường được xây dựng phù hợp với các nước phát triển
Nguồn dữ liệu để thực hiện những nghiên cứu phù hợp với từng quốc gia như:
- môi trường dịch tễ học
- môi trường vật lý;
- nguồn tài chính;
- bảo trì công nghệ
- Cơ sở hạ tầng dân dụng và y tế;
- nguồn nhân lực có tay nghề cao;
-Môi trường pháp lý;
- Các tiêu chuẩn chuyên môn y tế;
lợi nhuận của chăm sóc sức khỏe
-thị trường
[1] World Health Organization , Health technology assessment of medical devives, Switzerland, 2011
3. QUẢN LÍ CÔNG NGHỆ Y TẾ
"Xây dựng cho phù hợp
3. QUẢN LÍ CÔNG NGHỆ Y TẾ
"Xây dựng cho phù hợp
Giới thiệu quản lí công nghệ y tế ở Mỹ thông qua Cục quản lí thực phẩm và dược phẩm Hoa Kì (FDA) -cơ quan liên bang duy nhất được Quốc hội giao nhiệm vụ điều chỉnh các thiết bị y tế để đảm bảo an toàn và hiệu quả.Gồm các vấn đề:
- Quy định đổi mới về thiết bị y tế
- Bốn quy tắc chính để tiếp thị thiết bị y tế ở thị trường Mỹ
- Vấn đề đạo đức trong những nghiên cứu khả thi
- Y đức trong trường hợp cấp cứu.
- Vấn đề đạo đức trong sử dụng điều trị [2]
[1] World Health Organization , Health technology assessment of medical devives, Switzerland, 2011
[2] John D. Enderle, Joseph D. Bronzino , Introduction to Biomedical Engineering,Connecticut, 2011
3.1 QUY ĐỊNH ĐỔI MỚI VỀ THIẾT BỊ Y TẾ
1938:
3.1 QUY ĐỊNH ĐỔI MỚI VỀ THIẾT BỊ Y TẾ
1938:
1976: luật sửa đổi thiết bị y tế - bộ luật đầu tiên bắt buộc phải đánh giá các thiết bị y tế trước khi tung ra thị trường. Đạo luật này yêu cầu sự chấp thuận của FDA trước khi thiết bị mới được đưa ra thị trường và áp đặt các yêu cầu cho kiểm tra lâm sàng thiết bị y tế mới trên con người.
Trung tâm cho các thiết bị và phóng xạ trong y tế (CDRH) chịu trách nhiệm đảm bảo các an toàn và hiệu quả của các thiết bị y tế và loại bỏ tiếpxúc không cần thiết của con người với bức xạ từ y tế nhân tạo, lao động, và các sản phẩm tiêu dùng. CDRH có sáu văn phòng riêng biệt: văn phòng hệ thống và quản lý, văn phòng chính sách, văn phòng khoa học và công nghệ, văn phòng y tế và công nghiệp, văn phòng giám sát và sinh trắc học, và văn phòng đánh giá thiết bị (ODE).
[2] John D. Enderle, Joseph D. Bronzino , Introduction to Biomedical Engineering,Connecticut, 2011
3.2 BỐN QUY TẮC TIẾP THỊ THIẾT BỊ Y TẾ Ở
3.2 BỐN QUY TẮC TIẾP THỊ THIẾT BỊ Y TẾ Ở
1
2
3
4
Sự chấp thuận trước khi vào thị trường ( PMA)
Sự miễn kiểm tra thiết bị
(IDE)
Nghị định phát triển sản phẩm (PDP)
Thông báo 510(k)
[2] John D. Enderle, Joseph D. Bronzino , Introduction to Biomedical Engineering,Connecticut, 2011
3.3 VẤN ĐỀ ĐẠO ĐỨC TRONG NHỮNG NGHIÊN CỨU KHẢ THI
3.3 VẤN ĐỀ ĐẠO ĐỨC TRONG NHỮNG NGHIÊN CỨU KHẢ THI
Trong một nghiên cứu tính khả thi, hoặc "nghiên cứu hạn chế", nghiên cứu của con người liên quan đến việc sử dụng của một thiết bị mới sẽ diễn ra tại một tổ chức duy nhất và không có hơn mười đối tượng. Các nhà tài trợ của một nghiên cứu hạn chế yêu cầu nộp cho FDA một "Thông báo các giới hạn nghiên cứu, "trong đó bao gồm một mô tả của thiết bị, một bản tóm tắt mục đích của cuộc nghiên cứu, các giao thức, một giấy chứng nhận, và sự xác nhậncủa ủy ban y tế có thẩm quyền. Trong những trường hợp nhất định, FDA có thể yêu cầu thêm thông tin hoặc yêu cầu trình lên một ứng dụng IDE đầy đủ hoặc đình chỉ việc nghiên cứu.
Mặc dù khoa học là một điều kiện cần thiết của nghiên cứu đảm bảo đạo đức, nhưng nó chưa đủ. Yêu cầu này được đáp ứng bằng cách đảm bảo rằng không có người có thẩm quyền phải chịu bất cứ can thiệp lâm sang nào mà không có sự đồng ý tự nguyện. Hơn nữa, sự tôn trọng cho người có nghĩa rằng các bác sĩ sẽ không để bất cứ người nào chịu những rủi ro không cần thiết và ý giảm thiểu các rủi ro cho bệnh nhân trong các thủ tục cần thiết.
[2] John D. Enderle, Joseph D. Bronzino , Introduction to Biomedical Engineering,Connecticut, 2011
3.4 Y ĐỨC TRONG TRƯỜNG HỢP CẤP CỨU
Tổ chức sức
3.4 Y ĐỨC TRONG TRƯỜNG HỢP CẤP CỨU
Tổ chức sức
Mục đích của việc sử dụng khẩn cấp một thiết bị chưa được chấp thuận là để cố gắng cứu người sắp chết ,cuộc sống của bệnh nhân trong những hoàn cảnh mà không có cách nào khác để thay thế.
Tuy nhiên tổ chức y tế luôn yêu cầu các bác sĩ sử dụng các thiết bị chưa được kiểm duyệt này phải có lý do chính đáng minh chứng cho việc tồn tại của các lợi ích. Điều này có nghĩa là cần có một cơ thể của tiền lâm sàng và động vật đã kiểm tra cho phép một dự đoán là có các lợi ích có thể áp dụng cho một bệnh nhân như là con người.
Cũng đặc biệt quan trọng ở đây là bản chất của sự đồng ý của bệnh nhân cá nhân phải đối mặt với cái chết. Nó thật sự trở thành sự bốc lột trong thử nghiệm khi đó là trường hợp áp dụng chưa cần thiết và chưa phải là cách duy nhất.
[2] John D. Enderle, Joseph D. Bronzino , Introduction to Biomedical Engineering,Connecticut, 2011
3.5 VẤN ĐỀ ĐẠO ĐỨC TRONG SỬ DỤNG ĐIỀU TRỊ
Thứ hai
Tóm
3.5 VẤN ĐỀ ĐẠO ĐỨC TRONG SỬ DỤNG ĐIỀU TRỊ
Thứ hai
Tóm
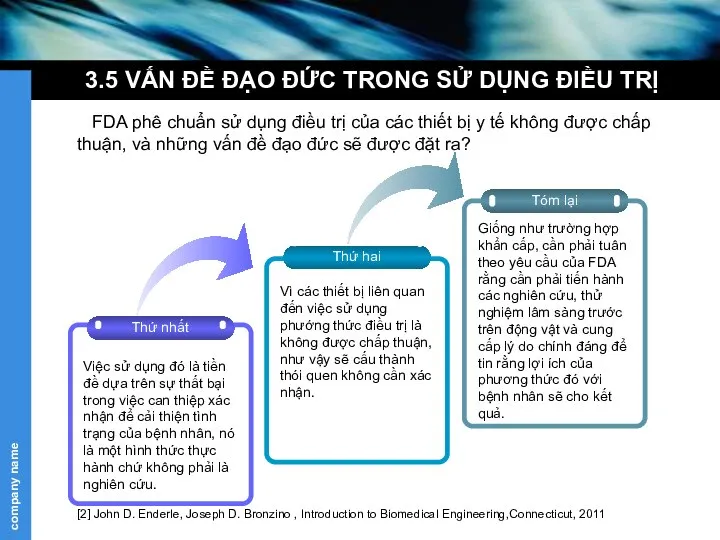
Vì các thiết bị liên quan đến việc sử dụng phướng thức điều trị là không được chấp thuận, như vậy sẽ cấu thành thói quen không cần xác nhận.
Giống như trường hợp khẩn cấp, cần phải tuân theo yêu cầu của FDA rằng cần phải tiến hành các nghiên cứu, thử nghiệm lâm sàng trước trên động vật và cung cấp lý do chính đáng để tin rằng lợi ích của phương thức đó với bệnh nhân sẽ cho kết quả.
FDA phê chuẩn sử dụng điều trị của các thiết bị y tế không được chấp thuận, và những vấn đề đạo đức sẽ được đặt ra?
Việc sử dụng đó là tiền đề dựa trên sự thất bại trong việc can thiệp xác nhận để cải thiện tình trạng của bệnh nhân, nó là một hình thức thực hành chứ không phải là nghiên cứu.
[2] John D. Enderle, Joseph D. Bronzino , Introduction to Biomedical Engineering,Connecticut, 2011
4.SO SÁNH ĐÁNH GIÁ VÀ QUẢN LÍ CNYT
[1] World Health Organization
4.SO SÁNH ĐÁNH GIÁ VÀ QUẢN LÍ CNYT
[1] World Health Organization
5.TÀI LIỆU THAM KHẢO
[1] World Health Organization , Health technology assessment
5.TÀI LIỆU THAM KHẢO
[1] World Health Organization , Health technology assessment
[2] John D. Enderle, Joseph D. Bronzino , Introduction to Biomedical Engineering,Connecticut, 2011


![2.ĐÁNH GIÁ CÔNG NGHỆ Y TẾ [1] World Health Organization ,](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1441700/slide-4.jpg)


![2.3 HỢP TÁC QUỐC TẾ TRONG ĐGCNYT [1] World Health Organization](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1441700/slide-7.jpg)






![4.SO SÁNH ĐÁNH GIÁ VÀ QUẢN LÍ CNYT [1] World Health](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1441700/slide-15.jpg)
![5.TÀI LIỆU THAM KHẢO [1] World Health Organization , Health technology](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1441700/slide-16.jpg)
 Сестринский процесс при ревматизме
Сестринский процесс при ревматизме Холестеатома среднего уха. Этиология. Патогенез
Холестеатома среднего уха. Этиология. Патогенез Многоформная экссудативная эритема
Многоформная экссудативная эритема Первинна, вторинна і третинна профілактика в стоматології
Первинна, вторинна і третинна профілактика в стоматології Структура заболеваемости. Асфиксия новорожденного
Структура заболеваемости. Асфиксия новорожденного Лечение пульпита. Классификация методов. Витальные и девитальные методы лечения пульпита. Ошибки и осложнения, их устранение
Лечение пульпита. Классификация методов. Витальные и девитальные методы лечения пульпита. Ошибки и осложнения, их устранение Оценка жизнедеятельности плода. Методы исследования. Патология беременности
Оценка жизнедеятельности плода. Методы исследования. Патология беременности Лечение периодонтита постоянных зубов. Выбор пломбировочного материала
Лечение периодонтита постоянных зубов. Выбор пломбировочного материала Реанимация. Тесты
Реанимация. Тесты Neurocognitive disorders
Neurocognitive disorders Физиология крови
Физиология крови М-холиноблокаторы
М-холиноблокаторы Кожно-пластическая бригада
Кожно-пластическая бригада Инсульт. Это важно знать!
Инсульт. Это важно знать! Нейссерии. Род Neisseria
Нейссерии. Род Neisseria Клиника и диагностика фибрилляции предсердий и желудочков сердца
Клиника и диагностика фибрилляции предсердий и желудочков сердца ВПС у новорожденных
ВПС у новорожденных Кожа и патологии
Кожа и патологии Дәрігер стоматологқа келген науқастарды седотивті емдеу
Дәрігер стоматологқа келген науқастарды седотивті емдеу Қарым-қатынас әдістері
Қарым-қатынас әдістері Плодоразрушающие операции
Плодоразрушающие операции Жүкті əйелдердің қан мен қанөндіру түзуші ағзаларының жəне иммундық механизмдердің
Жүкті əйелдердің қан мен қанөндіру түзуші ағзаларының жəне иммундық механизмдердің Тұқым қуалайтын аурулардың пайда болуының жалпы тетіктері, диагностика, алдын алу және емдеудің ұстанымдары
Тұқым қуалайтын аурулардың пайда болуының жалпы тетіктері, диагностика, алдын алу және емдеудің ұстанымдары Лучевая диагностика доброкачественных новообразований костей
Лучевая диагностика доброкачественных новообразований костей Сказки детства. Этапы отношений между мужчиной и женщиной
Сказки детства. Этапы отношений между мужчиной и женщиной Первичная профилактика сосудистой деменции
Первичная профилактика сосудистой деменции Введение в детскую терапию (по К. Бремс)
Введение в детскую терапию (по К. Бремс) Хронический гастрит. Язвенная болезнь желудка и двенадцатиперстной кишки. Хронический энтерит
Хронический гастрит. Язвенная болезнь желудка и двенадцатиперстной кишки. Хронический энтерит