Содержание
- 2. Потенциометрический метод анализа основан на использовании зависимости ЭДС электрохимической цепи от активности анализируемого иона. Потенциометрический метод
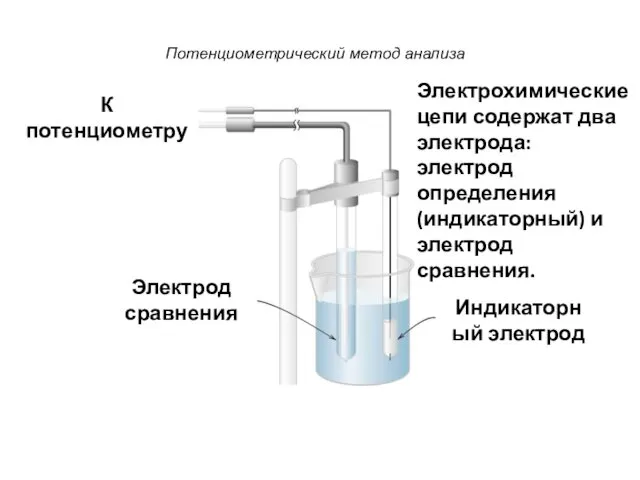
- 3. Потенциометрический метод анализа Электрод сравнения Индикаторный электрод К потенциометру Электрохимические цепи содержат два электрода: электрод определения
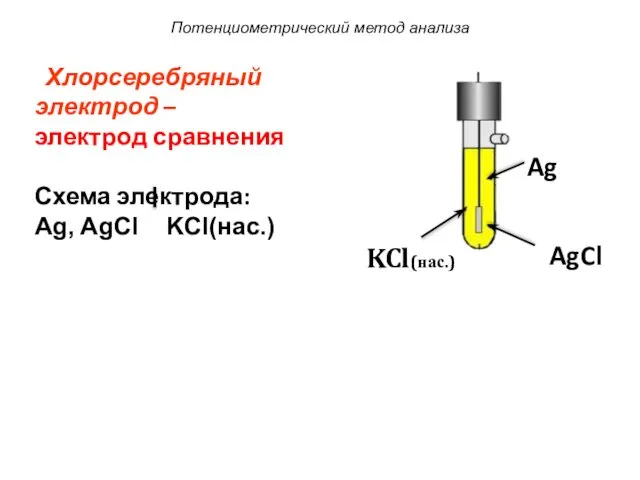
- 4. Потенциометрический метод анализа Ag AgCl KCl(нас.) Хлорсеребряный электрод – электрод сравнения Схема электрода: Ag, AgCl KCl(нас.)
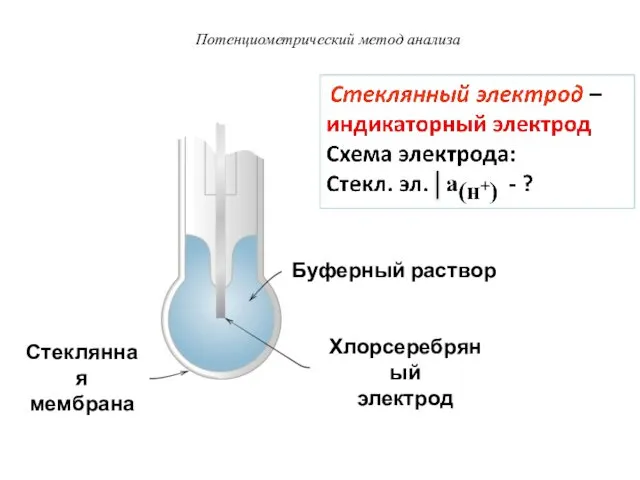
- 5. Потенциометрический метод анализа Стеклянная мембрана Хлорсеребряный электрод Буферный раствор
- 6. Потенциометрический метод анализа
- 7. Потенциометрический метод анализа Виды потенциометрического анализа: - прямая потенциометрия, или ионометрия; - потенциометрическое титрование. Метод прямой
- 8. Потенциометрический метод анализа Техника титрования: заполнение кончика бюретки Потенциометрическое титрование основано на определении точки эквивалентности по
- 9. Потенциометрический метод анализа Техника титрования
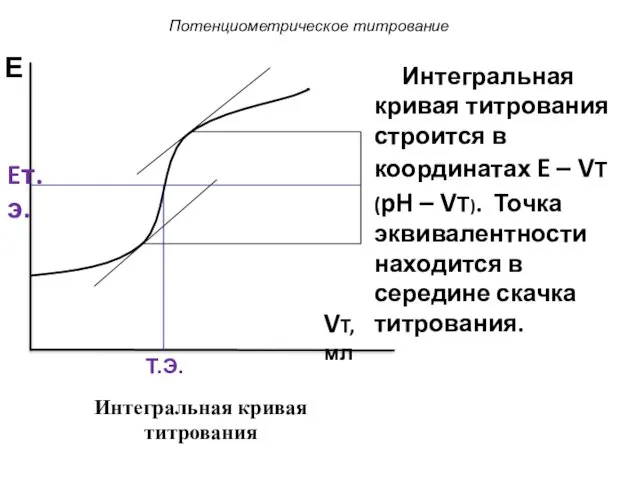
- 10. Потенциометрическое титрование VT, мл Интегральная кривая титрования строится в координатах E – VТ (pH – VТ).
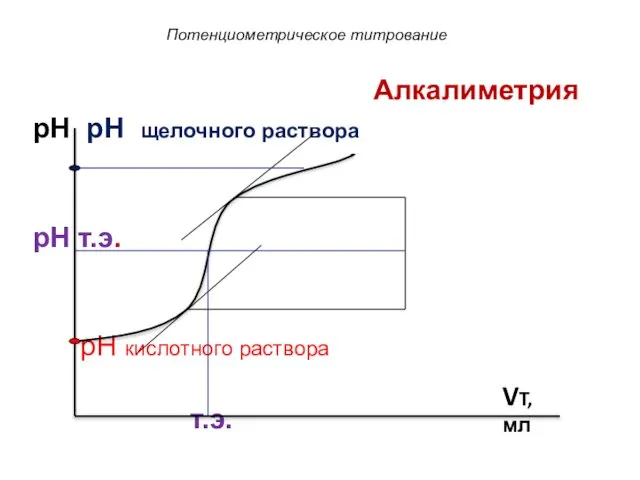
- 11. Потенциометрическое титрование pH pH щелочного раствора pH т.э. pH кислотного раствора т.э. VT, мл Алкалиметрия
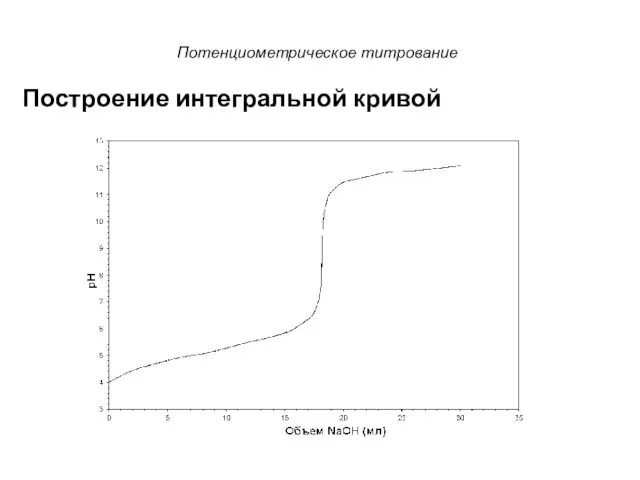
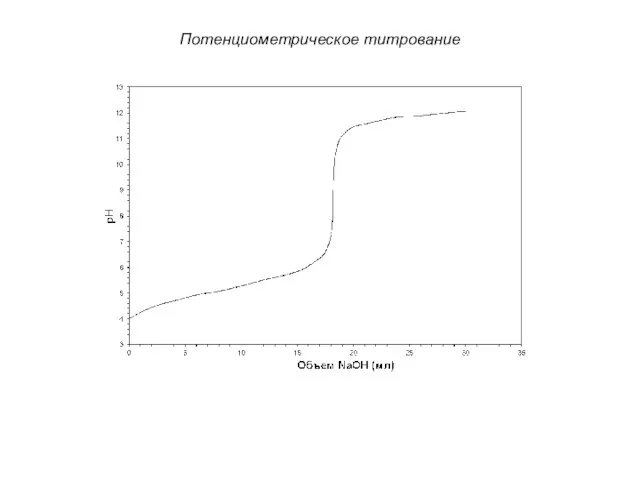
- 12. Потенциометрическое титрование Построение интегральной кривой
- 13. Потенциометрическое титрование В этом диапазоне pH изменяется незначительно из-за незначительного изменения H+ ионов.
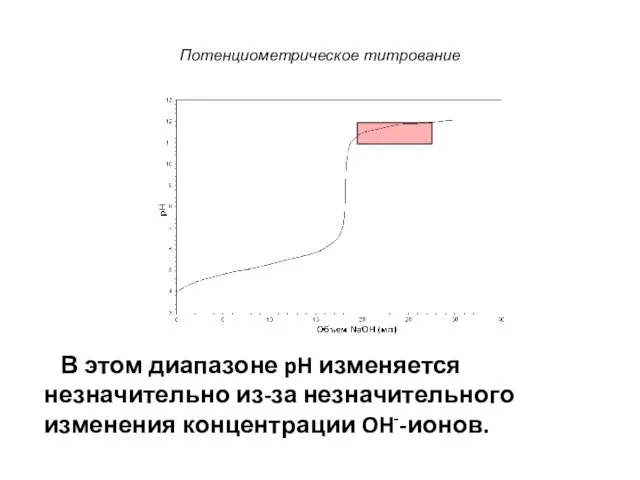
- 14. Потенциометрическое титрование В этом диапазоне pH изменяется незначительно из-за незначительного изменения концентрации OH--ионов.
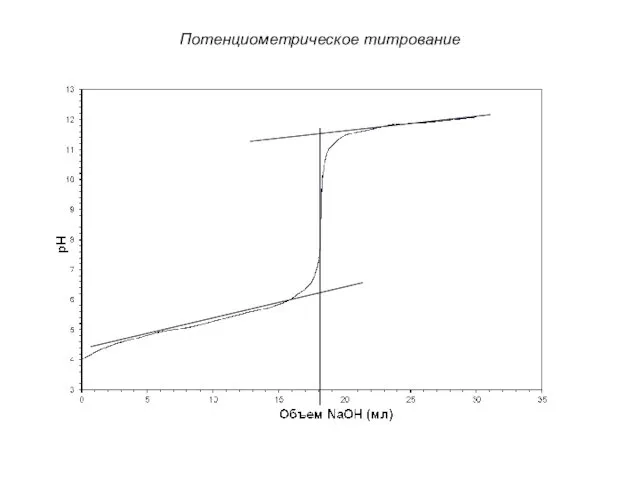
- 15. Потенциометрическое титрование
- 16. Потенциометрическое титрование
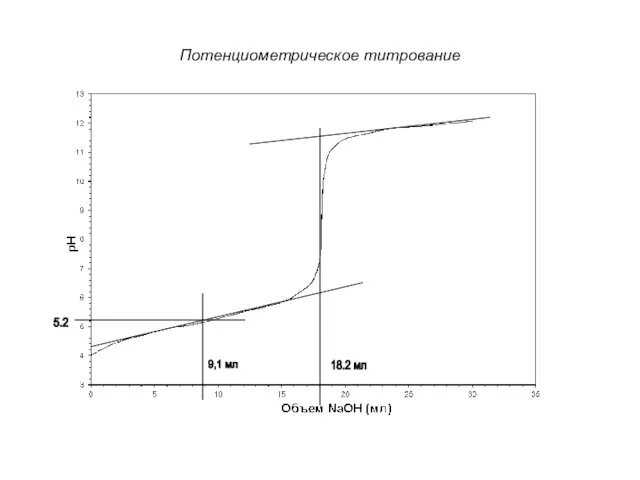
- 17. Потенциометрическое титрование 18.2 мл 9,1 мл 5.2
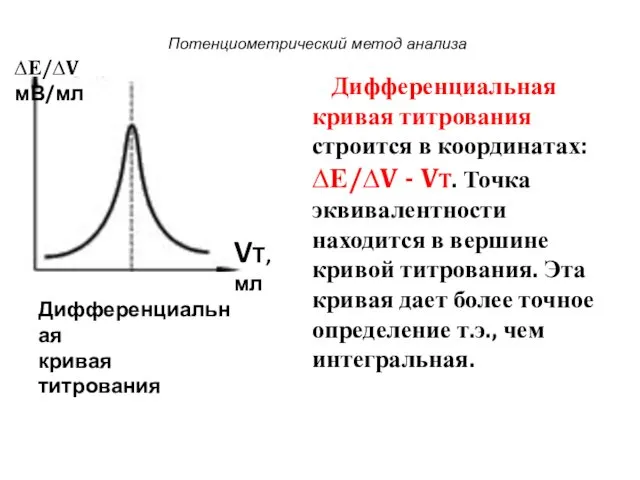
- 18. Потенциометрический метод анализа Дифференциальная кривая титрования строится в координатах: ∆Е/∆V - VT. Точка эквивалентности находится в
- 19. Потенциометрический метод анализа Количественные расчеты производят по закону эквивалентов: Метод потенциометрического титрования применяют при анализе мутных,
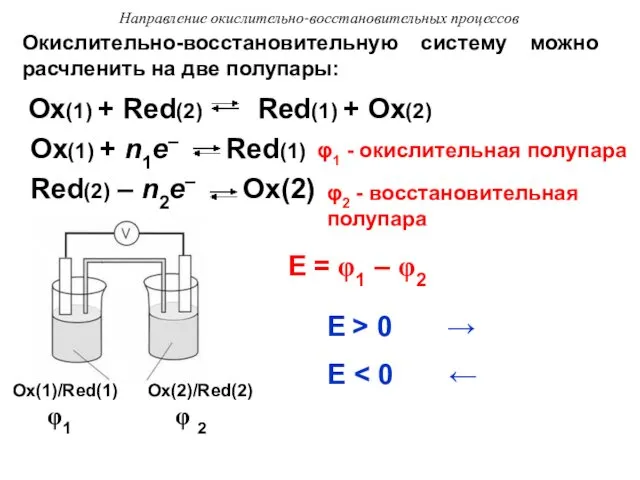
- 20. Направление окислительно-восстановительных процессов Окислительно-восстановительный процесс будет протекать в нужном направлении при условии, что разность электродных потенциалов
- 21. Направление окислительно-восстановительных процессов Оx(1) + Red(2) Red(1) + Оx(2) Оx(1) + n1e– Red(1) Red(2) – n2e–
- 22. Часто вместо таких полупар рассматривают две полуреакции, в которые включают не только атомы, изменяющие свою степень
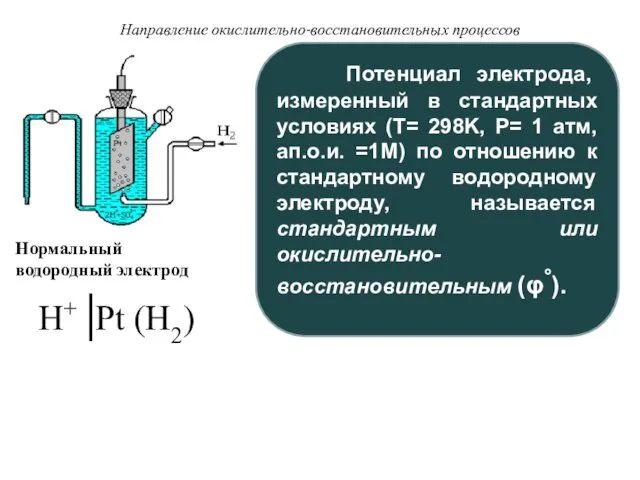
- 23. Направление окислительно-восстановительных процессов Потенциал электрода, измеренный в стандартных условиях (T= 298K, P= 1 атм, ап.о.и. =1M)
- 24. Направление окислительно-восстановительных процессов Оx + Н2 Red + 2Н+ Е° = φ°(Оx/Red) – φ°(Н+/1/2Н2) = φ°(Оx/Red)
- 25. Направление окислительно-восстановительных процессов Окислительно-восстановительный процесс протекает в прямом направлении до конца при любых начальных условиях, если
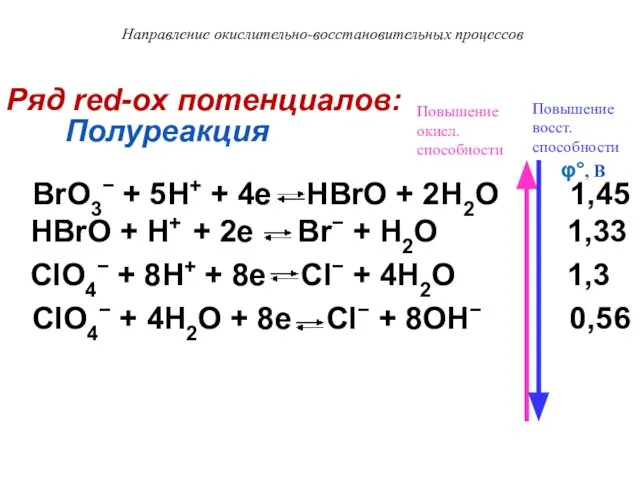
- 26. Направление окислительно-восстановительных процессов Чем выше значение стандартного электродного потенциала φ0, тем выше у данной полупары окислительная
- 27. Ряд red-ox потенциалов: Полуреакция BrO3− + 5H+ + 4e HBrO + 2H2O 1,45 HBrO + H+
- 28. Направление окислительно-восстановительных процессов Например: Сd2+ + 2e- Cd0, IO3- + 6H+ + 6e- I- + 3Н2О,
- 29. Направление окислительно-восстановительных процессов Первая система является системой восстановителя. На этом электроде будет протекать процесс отдачи электронов
- 30. Направление окислительно-восстановительных процессов Суммарное уравнение реакции: Cd0 - 2e- Сd2+ 3 IO3- + 6H+ + 6e-
- 31. Направление окислительно-восстановительных процессов Гальваническая цепь: Cd0 Сd2+ IO3-, H+ Pt I- Е = φ° IO3-/I- -
- 32. Направление окислительно-восстановительных процессов Cd2+ (р) + 2e- Cd (т) φ0 = -0,40 В Cd2+ - окислитель,
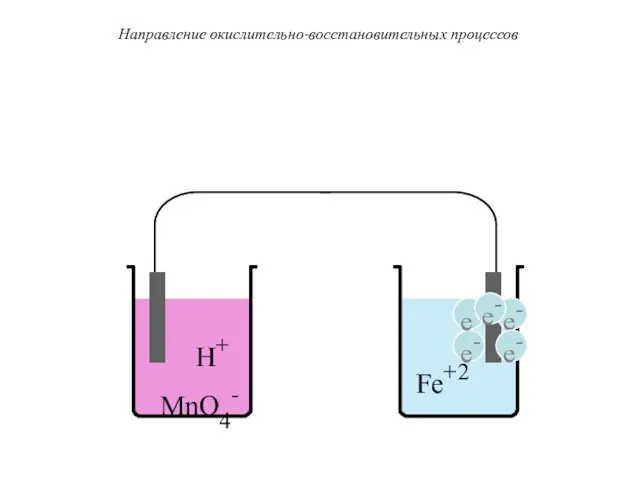
- 33. Направление окислительно-восстановительных процессов Например: MnO4- + 8H+ + 5e- Mn+2 + 4H2O, φ0 MnO4-, H+/Mn+2 =
- 34. H+ MnO4- Fe+2 Направление окислительно-восстановительных процессов
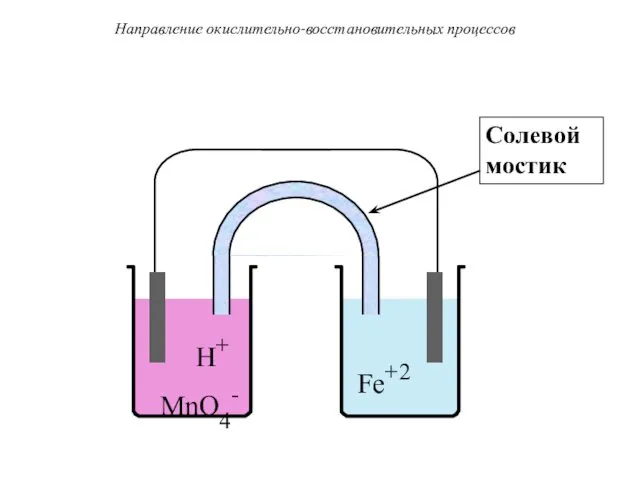
- 35. H+ MnO4- Fe+2 Направление окислительно-восстановительных процессов Солевой мостик
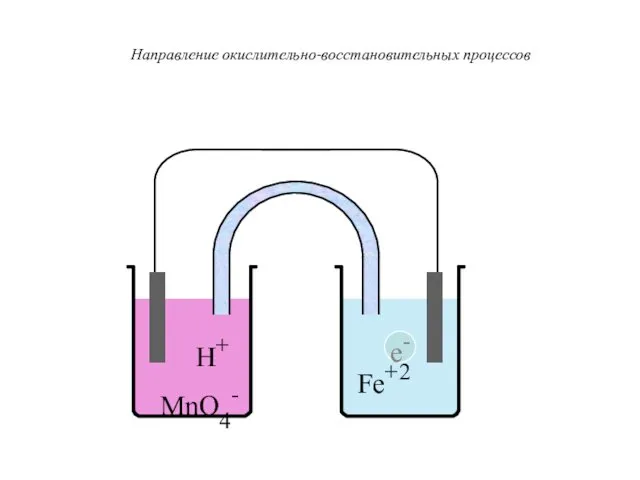
- 36. H+ MnO4- Fe+2 Направление окислительно-восстановительных процессов
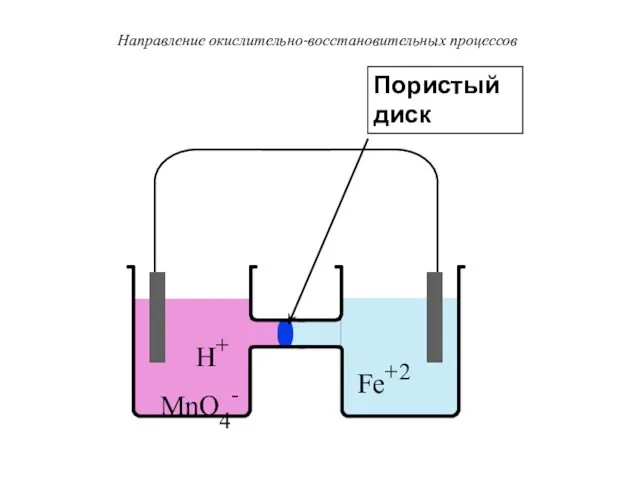
- 37. H+ MnO4- Fe+2 Пористый диск Направление окислительно-восстановительных процессов
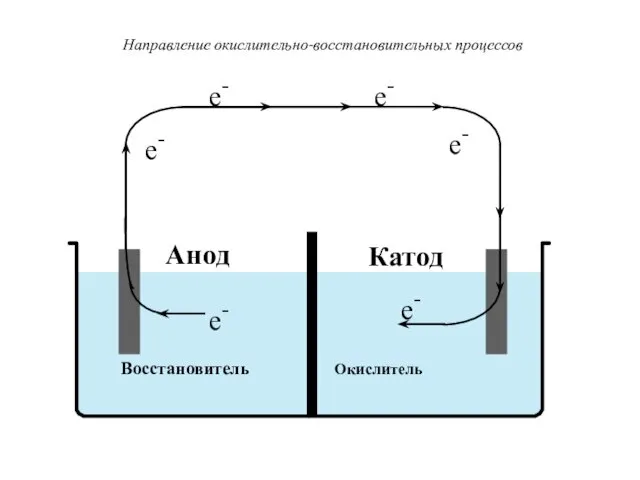
- 38. Восстановитель Окислитель e- e- e- e- e- e- Анод Катод Направление окислительно-восстановительных процессов
- 39. Направление окислительно-восстановительных процессов Первая система является системой окислителя. На этом электроде будет протекать процесс присоединения электронов
- 40. Направление окислительно-восстановительных процессов Суммарное уравнение реакции: MnO4- + 8H+ + 5e- → Mn+2 + 4H2O 1
- 41. Направление окислительно-восстановительных процессов
- 42. В гальванических элементах протекают необратимые реакции: их нельзя перезаряжать и можно использовать однократно. Химические источники тока,
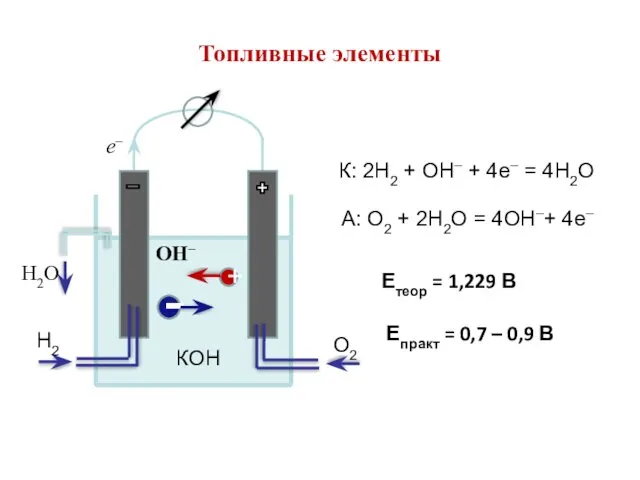
- 43. К: 2Н2 + ОН– + 4е– = 4Н2О А: О2 + 2Н2О = 4ОН–+ 4е– Топливные
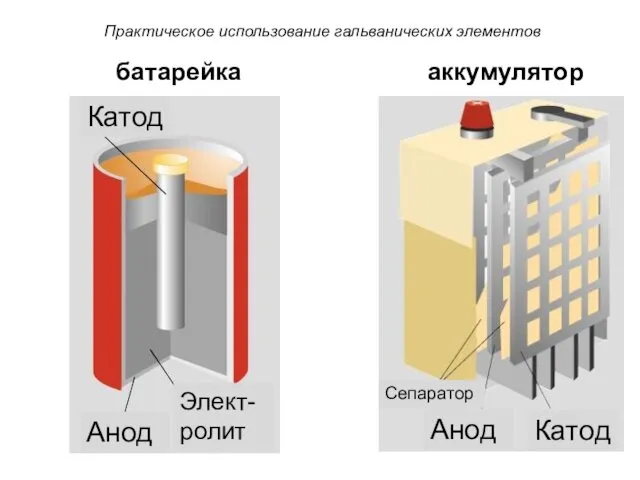
- 44. Практическое использование гальванических элементов батарейка аккумулятор Катод Анод Сепаратор Анод Элект-ролит Катод
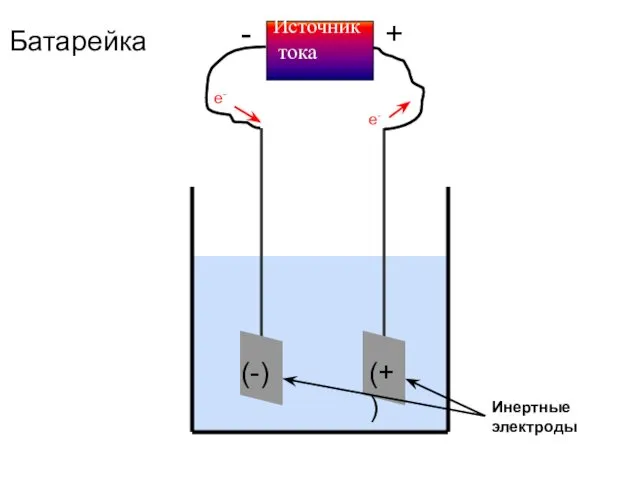
- 45. Источник тока + - Инертные электроды e- e- Батарейка (-) (+)
- 46. Химические процессы при электролизе расплава хлорида натрия, NaCl? Na+ Cl-
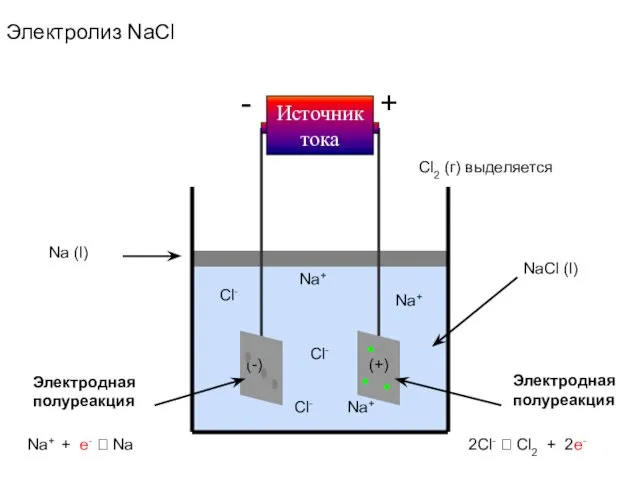
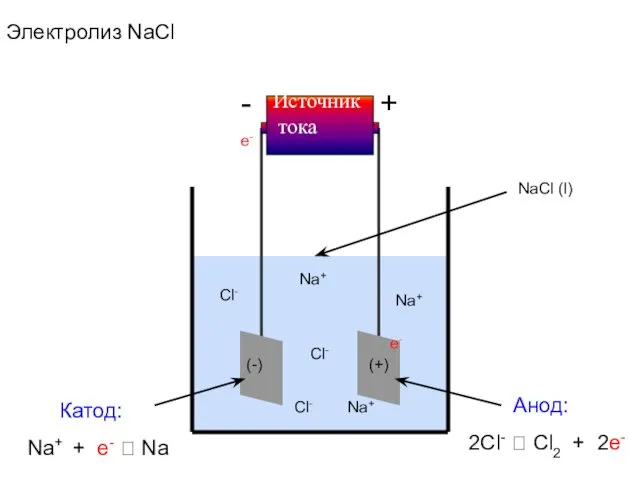
- 47. + - Источник тока Na (l) Электродная полуреакция Электродная полуреакция Электролиз NaCl Na+ Cl- Cl- Na+
- 48. + - Источник тока e- e- NaCl (l) (-) (+) Катод: Анод: Электролиз NaCl Na+ Cl-
- 49. Электродные процессы Катод (-) ВОССТАНОВЛЕНИЕ Na+ + e- ? Na Анод (+) ОКИСЛЕНИЕ 2Cl- ? Cl2
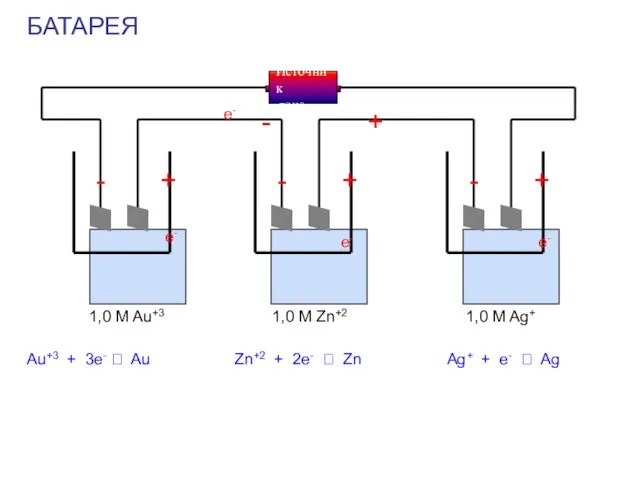
- 50. БАТАРЕЯ - + + + + - - - 1,0 M Au+3 1,0 M Zn+2 1,0
- 51. Вопросы для самоконтроля Сформулируйте правило «правого плюса». Укажите области применения гальванических элементов. В чем сущность потенциометрического
- 53. Скачать презентацию
























 Адреноблокаторы
Адреноблокаторы Реставрация костного препарата (черепа)
Реставрация костного препарата (черепа) Электрофорез. Иммунотипирование в капиллярном электрофорезе
Электрофорез. Иммунотипирование в капиллярном электрофорезе Рефракция и аккомодация глаза
Рефракция и аккомодация глаза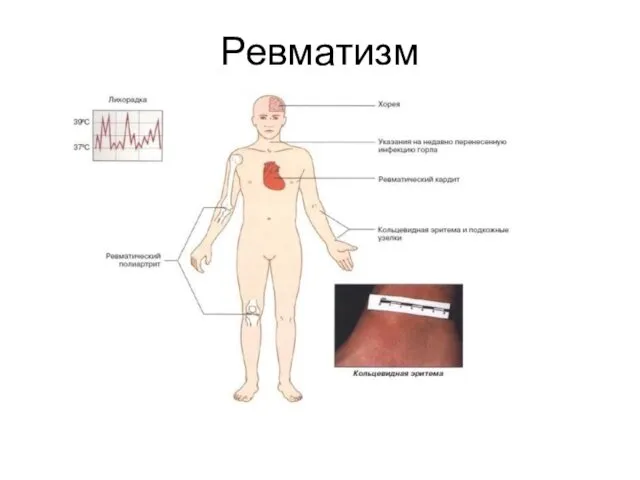 Острая ревматическая лихорадка
Острая ревматическая лихорадка Создание творческой мастерской «Каракули» для людей с психическими заболеваниями города Кондопога при КРОО «Преодоление»
Создание творческой мастерской «Каракули» для людей с психическими заболеваниями города Кондопога при КРОО «Преодоление» Патофизиология сердечно-сосудистой системы
Патофизиология сердечно-сосудистой системы Ревматоидты артрит
Ревматоидты артрит СРС: Балалардағы сарып. Клиникалық протокол
СРС: Балалардағы сарып. Клиникалық протокол Периметрия. Основные понятия
Периметрия. Основные понятия Человек. Индивид. Личность
Человек. Индивид. Личность Психология и педагогика
Психология и педагогика Эпидемиологические аспекты онкологической патологии, нервнопсихические заболевания
Эпидемиологические аспекты онкологической патологии, нервнопсихические заболевания Катаракта глаз
Катаракта глаз Изоспорозы. Токсоплазмоз
Изоспорозы. Токсоплазмоз Энтеральные вирусные гепатиты А и Е
Энтеральные вирусные гепатиты А и Е The Most Feared Disease of the 19th Century
The Most Feared Disease of the 19th Century Рентгенография. С какой целью проводится рентгенография. Подготовка к прохождению
Рентгенография. С какой целью проводится рентгенография. Подготовка к прохождению Плацентарная недостаточность: перспективы профилактики, диагностики и лечения
Плацентарная недостаточность: перспективы профилактики, диагностики и лечения Шигеллезы. Учебно-методическое пособие для студентов V курса педфака
Шигеллезы. Учебно-методическое пособие для студентов V курса педфака Seberealizace
Seberealizace Фармацевтическая опека. Простуда, ОРВИ
Фармацевтическая опека. Простуда, ОРВИ Средства, действующие преимущественно на ЦНС. Анальгетические, противосудорожные и противопаркинсонические лекрственные средства
Средства, действующие преимущественно на ЦНС. Анальгетические, противосудорожные и противопаркинсонические лекрственные средства Керамические материалы, применяемые в ортопедической стоматологии
Керамические материалы, применяемые в ортопедической стоматологии Алиментарные заболевания. Классификация. Заболевания, связанные с недостаточным и избыточным питанием
Алиментарные заболевания. Классификация. Заболевания, связанные с недостаточным и избыточным питанием CAR-T клетки
CAR-T клетки Нейродегенеративті аурулардың биохимиялық негіздері. Жұлын сұйықтығы:оны зерттеудің диагностикалық маңызы
Нейродегенеративті аурулардың биохимиялық негіздері. Жұлын сұйықтығы:оны зерттеудің диагностикалық маңызы Сестринское дело во фтизиатрии
Сестринское дело во фтизиатрии