Содержание
- 2. Источник. Семинар «Квалификация и валидация в рамках действующих и перспективных правил GMP» 23-24.09.2019 Компания «Виалек». https://cub.biocad.ru/knowbase/knowbase/view?id=4655
- 3. Приказ Минпромторга России от 14.06.2013 N916 (ред. от 18.12.2015) "Об утверждении Правил надлежащей производственной практик». ICH
- 4. Требования GMP к валидации
- 5. 1.4 Фармацевтическая система качества предназначенная для производства лекарственных средств, должна гарантировать что: х) проведенный весь необходимый
- 6. Фармацевтическая система качества Правила: Любая работающая сложная система развивается на базе работающей простой системы. Сложная система
- 7. Жизненный цикл лекарств
- 8. Критические атрибуты качества (CQA) Это физические, химические, биологические, или микробиологические свойства или характеристики которые должны быть
- 9. Трансфер технологии Цель: передача знаний о продукте и процессе между разработкой и производством, и между производственными
- 10. Требования GMP. Часть 1 Технологический процесс. Предотвращение перекрёстного загрязнения 5.21 Технические средства xii) использование автоматических систем
- 11. Валидация очистки 10.1 Должна выполняться валидация очистки для того, чтобы подтвердить эффективность любой процедуры очистки для
- 12. ОБЩАЯ ИНФОРМАЦИЯ. Управление рисками для качества должно использоваться на протяжении всего жизненного цикла лекарственного средства. В
- 13. Анализ рисков Анализ рисков является одним из примеров применения для оценки вариабельности процесса на протяжении жизненного
- 14. 2. ДОКУМЕНТАЦИЯ, ВКЛЮЧАЯ ПЛАН ВАЛИДАЦИИ 2.1 Надлежащая документация является основой для управления знаниями на протяжении жизненного
- 15. Требования GMP. Приложение 15 3. ЭТАПЫ КВАЛИФИКАЦИИ ОБОРУДОВАНИЯ, ОБЪЕКТОВ И ИНЖЕНЕРНЫХ СИСТЕМ 3.1 Квалификационные мероприятия должны
- 16. V модель проведения квалификации
- 17. Жизненный цикл квалификации
- 18. 5. ВАЛИДАЦИЯ ПРОЦЕССА 5.4 Валидация процесса, проводимая для нового препарата, должна охватывать все выпускаемые на рынок
- 19. Сопутствующая валидация 5.16 В исключительных случаях, когда польза от применения препарата значительно превышает сопутствующий риск для
- 20. Традиционная валидация процесса 5.18 Традиционный подход предусматривает производство некоторого количества серий готового продукта в условиях рутинного
- 21. Непрерывная верификация процесса 5.23 В случае применения для разработки препаратов подхода «спланированного качества» (QbyD), а также
- 22. Гибридный подход 5.26 В случае хорошо известных и полностью изученных препаратов и процессов, а также при
- 23. Текущая верификация процесса на протяжении жизненного цикла 5.29 Производители должны организовать мониторинг качества препарата для обеспечения
- 24. PPQ – квалификация производственного процесса Стратегия валидации производственного процесса
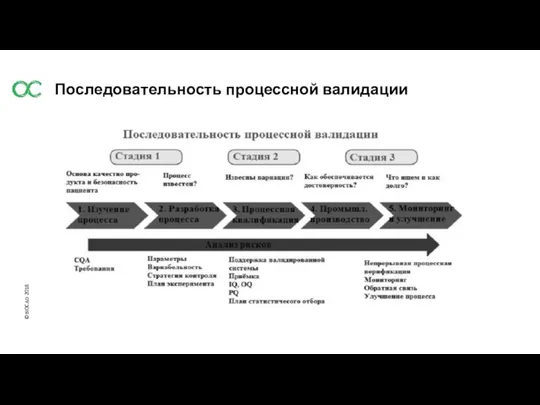
- 25. Последовательность процессной валидации
- 26. Программа мониторинга Программа непрерывной процессной верификации обеспечивает гарантию, что процесс находится в контролируемом состоянии после успешной
- 27. Рутинный отбор проб является источником данных для непрерывной верификации, но не рутинный отбор также должен выполнятся.
- 28. Частота обзора данных будет зависеть от величины риска для процессов и под‐процессов и охватывания контролем. Ежегодно
- 29. Анализ данных и трендовый анализ План непрерывной верификации должен чётко устанавливать как данные будут собраны и
- 30. Наиболее широко используется для валидации. Основной принцип – используемый отбор проб должен обеспечивать более высокую достоверность
- 31. Статистический контроль процесса Статистический контроль процесса (SPC) может использоваться для оценки, если процесс стабилен, предсказуемый и
- 32. гистограммы и точечные диаграммы диаграмма рассеивания временная диаграмма контрольные карты медиана –центральное значение для выборки объема
- 33. Контрольные карты Контрольные карты для переменных данных: • Х/R и X/S карты Шухарта с использованием пределов
- 34. Требования GMP. Часть 1 9. Обзоры качества 1.10 Необходимо проводить регулярные периодические обзоры качества всех зарегистрированных
- 35. Требования GMP. Часть 1 10. Управление знаниями Целью менеджмента знаний является не только сбор данных. Он
- 36. Аналитические методики Аналитические методы должны быть пригодны для их предполагаемой цели, обоснованы и воспроизводимы. Должна быть
- 38. Скачать презентацию


































 Вакцинация и иммунизация
Вакцинация и иммунизация Клиническая фармакология лекарственных средств, влияющих на сосудистый тонус
Клиническая фармакология лекарственных средств, влияющих на сосудистый тонус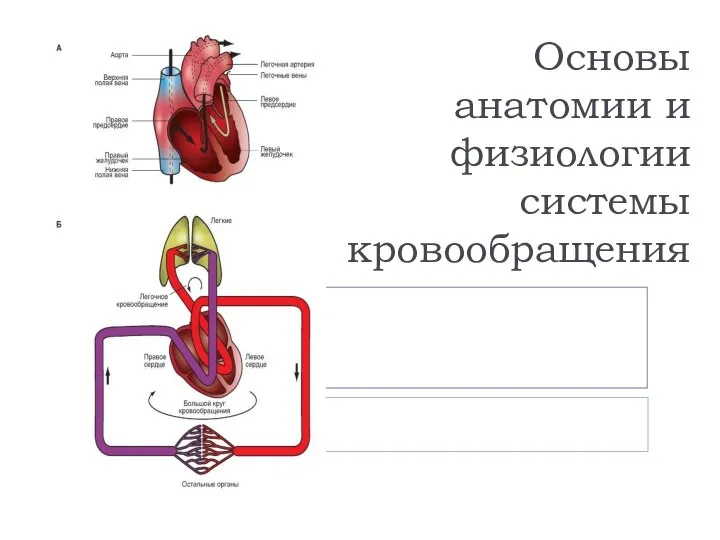 Основы анатомии и физиологии системы кровообращения
Основы анатомии и физиологии системы кровообращения Опухолевый рост
Опухолевый рост Анатомия как наука изучает форму и структуру организма человека
Анатомия как наука изучает форму и структуру организма человека Ұйқы безі ауруларының патоморфологиялық сипаттамасы
Ұйқы безі ауруларының патоморфологиялық сипаттамасы TQM в медицине. Необходимость управления качеством (СМК)
TQM в медицине. Необходимость управления качеством (СМК) Организация и принципы работы отделений анестезиологии, реаниматологии и интенсивной терапии
Организация и принципы работы отделений анестезиологии, реаниматологии и интенсивной терапии Основы генной терапии. Лечение врожденных иммунологических заболеваний – препарат Strimvelis
Основы генной терапии. Лечение врожденных иммунологических заболеваний – препарат Strimvelis Участие медицинской сестры в реабилитационных мероприятиях у пациентов с артрозами
Участие медицинской сестры в реабилитационных мероприятиях у пациентов с артрозами Жедел бүйрек жеткіліксіздігі. ЖБЖ-де бүйрек алмастыру терапиясы
Жедел бүйрек жеткіліксіздігі. ЖБЖ-де бүйрек алмастыру терапиясы Презентация по медицине Электротерапия
Презентация по медицине Электротерапия  Перфоративная язва желудка и двенадцатиперстной кишки
Перфоративная язва желудка и двенадцатиперстной кишки История развития психопатологии в зарубежных странах
История развития психопатологии в зарубежных странах Наркомания
Наркомания Болезнь Рейно
Болезнь Рейно Носовые кровотечения
Носовые кровотечения Фобии, депрессии, панические атаки - психокоррекция в неклиническом консультировании
Фобии, депрессии, панические атаки - психокоррекция в неклиническом консультировании Иммобилизденген ферменттер
Иммобилизденген ферменттер Шетелдік денсаулық сақтау
Шетелдік денсаулық сақтау Особенности клинического течения и выбора тактики хирургического лечения ДТЗ
Особенности клинического течения и выбора тактики хирургического лечения ДТЗ История медицины
История медицины Амилоидоз почек. Диагностика. Принципы лечения
Амилоидоз почек. Диагностика. Принципы лечения Алкоголизм. Профилактика алкоголизма
Алкоголизм. Профилактика алкоголизма Скрининг в онкологии
Скрининг в онкологии Влияние звуковых волн на слух человека
Влияние звуковых волн на слух человека Субтотальная гистерэктомия без придатков
Субтотальная гистерэктомия без придатков Герпетический энцефалит
Герпетический энцефалит