Содержание
- 2. Процесс разработки и продвижения на рынок нового препарата составляет в среднем 12–15 лет. Рост затрат на
- 3. В недалеком прошлом основным методом изыскания новых лекарственных средств был элементарный эмпирический скрининг уже имеющихся или
- 4. Современные высокотехнологические подходы подразумевают использование НTS–метода (High Through-put Screening), т.е. метода эмпирического конструирования нового высокоэффективного лекарственного
- 5. На втором этапе происходит непосредственное моделирование структурной активности с помощью специальных программ типа QSAR (Quantitative Structure
- 6. Как только перспективное химическое соединение синтезировано, а его структура и свойства установлены, приступают к доклиническому этапу
- 8. Для фармакодинамики — это исследование специфической фармакологической активности препарата и его метаболитов (включая определение скорости, продолжительности,
- 9. Доклинические исследования (I этап) (Отбор перспективных субстанций) 1. Оценка патентных возможностей и подача заявления на получение
- 10. Доклинические исследования (II этап) (Фармакодинамика/кинетика у животных) 1. Детальные фармакологические исследования (основное действие, нежелательные реакции, длительность
- 11. Доклинические исследования (III этап) (Оценка безопасности) 1. Острая токсичность (однократное введение двум видам животных). 2. Хроническая
- 12. Доклинические исследования (IV этап) (Ранняя техническая разработка) 1. Синтез в условиях производства. 2. Разработка аналитических методов
- 13. Прежде чем разработчик получит разрешение на проведение клинических испытаний, он должен представить в разрешительные органы заявку,
- 15. Программа клинических испытаний нового лекарственного средства на человеке состоит из четырех фаз. Первые три проводятся до
- 16. НЕСКОЛЬКО ТЕРМИНОВ Рандомизацией называется способ назначения испытуемых в группы методом случайной выборки (желательно с использованием компьютерных
- 17. 1-я фаза клинических испытаний. Часто эта фаза называется также медико-биологической, или клинико-фармакологической, что более адекватно отражает
- 18. 2-я фаза клинических испытаний — первый опыт применения нового препарата для лечения конкретной патологии. Часто эту
- 19. 3-я фаза клинических испытаний – это клинические исследования безопасности и эффективности препарата в условиях, приближенных к
- 20. 4-я фаза клинических испытаний – это так называемые постмаркетинговые, или пострегистрационные, исследования, проводимые после получения разрешения
- 21. СХЕМАТИЧНО ВСЕ ВЫШЕСКАЗАННОЕ ПРЕДСТАВЛЕНО НА РИСУНКЕ.
- 22. Элементы дизайна стандартного клинического исследования представлены следующим образом: наличие медицинского вмешательства; наличие группы сравнения; рандомизация; стратификация;
- 23. 1) Схема модели исследования в одной группе: все исследуемые получают одно и то же лечение, однако
- 24. 2) Схема модели исследования в параллельных группах: испытуемые двух или более групп получают различные курсы лечения
- 25. 3) Схема перекрестной модели: испытуемых рандомизируют в группы, в которых проводят одинаковое курсовое лечение, но с
- 27. СТОИМОСТЬ ПРОВЕДЕНИЯ КЛИНИЧЕСКИХ ИСПЫТАНИЙ И ВЫВЕДЕНИЯ НОВОГО ПРЕПАРАТА НА РЫНОК ЯВЛЯЕТСЯ ЦЕНТРАЛЬНОЙ ПРОБЛЕМОЙ ФАРМАЦЕВТИЧЕСКИХ КОМПАНИЙ!
- 28. Несмотря на очевидное понимание стоимости разработки препаратов и факторов, ответственных за эту стоимость, существует удивительный разброс
- 29. АНАЛИЗ Данные об 726 интервенционных исследованиях, проведенных в период с 2010 по 2015, были непосредственно получены
- 30. Этот всеохватывающий подход облегчает трудности, связанные с более традиционным сравнительным анализом, который был доступен ранее. Например,
- 32. Эти данные позволяют оценивать эффективность затрат тремя способами: во-первых, сравнением сфер затрат на клинические испытания компании
- 33. СРЕДНИЕ СТОИМОСТИ КЛИНИЧЕСКИХ ИСПЫТАНИЙ.
- 34. Для первого типа оценки могут быть использованы данные о средней стоимости каждой фазы клинических испытаний. Если
- 35. Для испытаний в наборе данных медианная стоимость проведения исследования (от утверждения протокола до окончательного отчета о
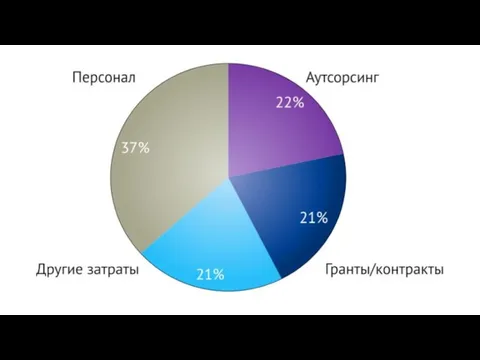
- 36. ВЛИЯНИЕ РАЗЛИЧНЫХ ФАКТОРОВ НА СТОИМОСТЬ
- 37. ПОКАЗАТЕЛИ ЭФФЕКТИВНОСТИ. Разница в эффективности работы (±1 стандартное отклонение) между компаниями по исследуемому набору данных соответствует
- 39. Скачать презентацию

































 Бас ми ісінуі
Бас ми ісінуі Вторичная артериальная гипертензия при эндокринной патологии надпочечников
Вторичная артериальная гипертензия при эндокринной патологии надпочечников Бактериальные кератиты. Дифференциальная диагностика. Лечение
Бактериальные кератиты. Дифференциальная диагностика. Лечение Управлінські конфлікти: типи, причини, шляхи вирішення та попередження
Управлінські конфлікти: типи, причини, шляхи вирішення та попередження Санитарно-гигиеническая характеристика экспертизы объекта Адмиралтейские верфи
Санитарно-гигиеническая характеристика экспертизы объекта Адмиралтейские верфи Дискурсивное поведение мужчин и женщин
Дискурсивное поведение мужчин и женщин День медика. Хирургия
День медика. Хирургия Медицина катастроф
Медицина катастроф Подкожная инъекция
Подкожная инъекция Неврологические симптомы и синдромы. Сестринский уход в невропатологии
Неврологические симптомы и синдромы. Сестринский уход в невропатологии Воспалительные заболевания мочеполовых органов
Воспалительные заболевания мочеполовых органов Сравнение конструктивистского и экологического подходов
Сравнение конструктивистского и экологического подходов Консультирование тревожных клиентов
Консультирование тревожных клиентов Дисфункциональные маточные кровотечения. Диагноз исключения
Дисфункциональные маточные кровотечения. Диагноз исключения Ингибиторы тирозинкиназ
Ингибиторы тирозинкиназ Создание единого цифрового контура в здравоохранении на основе ЕГИСЗ
Создание единого цифрового контура в здравоохранении на основе ЕГИСЗ Развитие зуба
Развитие зуба Острый аппендицит, аппендикулярный инфильтрат, периаппендикулярный абцесс, перитонит, пельвиоперитонит
Острый аппендицит, аппендикулярный инфильтрат, периаппендикулярный абцесс, перитонит, пельвиоперитонит Роль продуктов функционального питания в диетотерапии онкологических пациентов
Роль продуктов функционального питания в диетотерапии онкологических пациентов Полиомиелит
Полиомиелит Хронический геморрой
Хронический геморрой Токсикология. Основные разделы клинической токсикологии
Токсикология. Основные разделы клинической токсикологии Возрастные особенности детей 5-6 лет
Возрастные особенности детей 5-6 лет Кожный зуд
Кожный зуд Трещина прямой кишки
Трещина прямой кишки Адгезивная фиксация цельнокерамических вкладок, виниров и коронок
Адгезивная фиксация цельнокерамических вкладок, виниров и коронок Дыхание. Рак лёгких
Дыхание. Рак лёгких Комплексная диагностика кандидатов в замещающие родители
Комплексная диагностика кандидатов в замещающие родители