Содержание
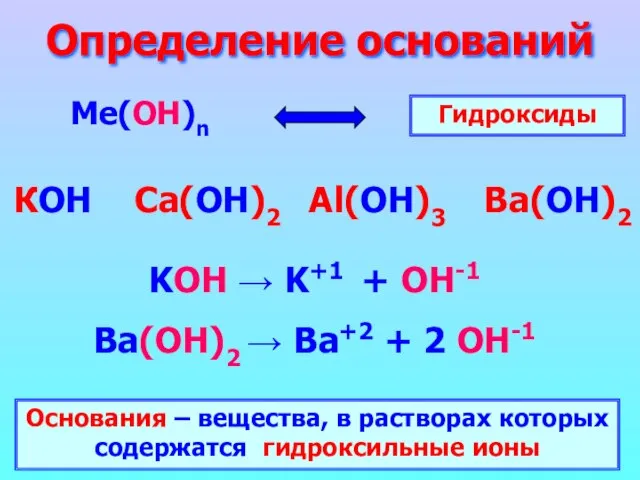
- 2. Определение оснований Ме(ОН)n КОН Ca(ОН)2 Al(ОН)3 Ba(ОН)2 Гидроксиды KOH → K+1 + OH-1 Ba(ОН)2 → Ba+2
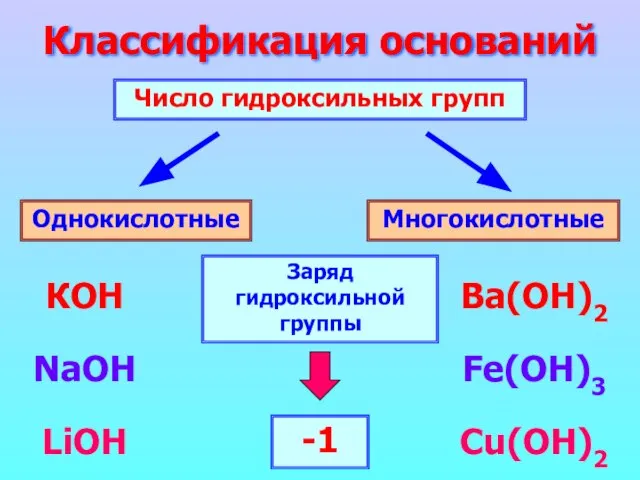
- 3. Классификация оснований Число гидроксильных групп Однокислотные Многокислотные КОН NaOH LiOH Ba(ОН)2 Fe(OH)3 Cu(OH)2 Заряд гидроксильной группы
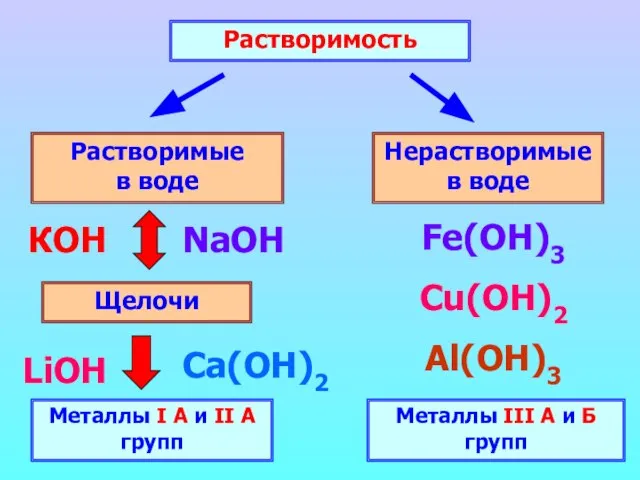
- 4. Растворимость Растворимые в воде Нерастворимые в воде Щелочи Металлы I А и II А групп КОН
- 5. Сильные и слабые основания
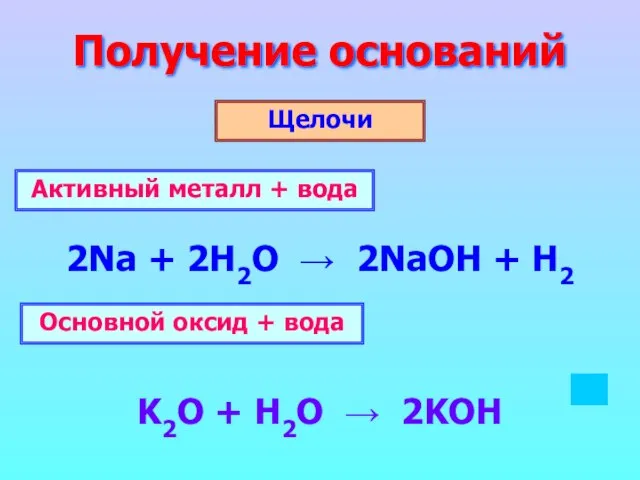
- 6. Получение оснований Щелочи 2Na + 2H2O → 2NaOH + H2 K2O + H2O → 2KOH Активный
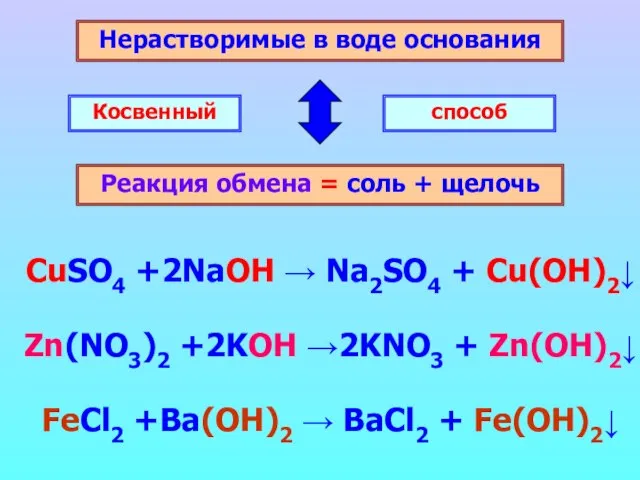
- 7. Нерастворимые в воде основания Реакция обмена = соль + щелочь Косвенный способ CuSO4 +2NaOH → Na2SO4
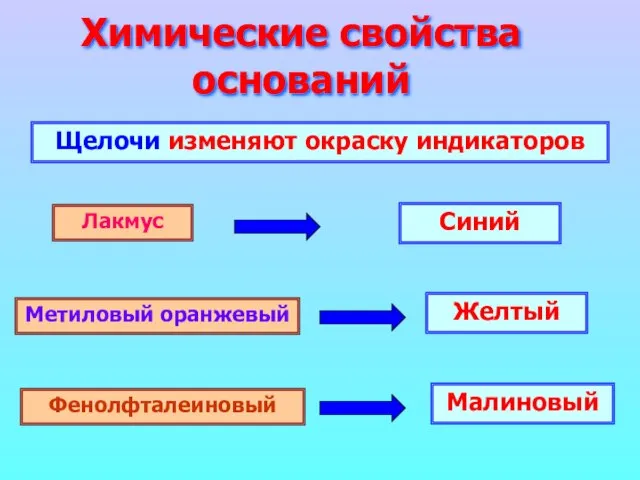
- 8. Химические свойства оснований Щелочи изменяют окраску индикаторов Лакмус Метиловый оранжевый Фенолфталеиновый Синий Желтый Малиновый
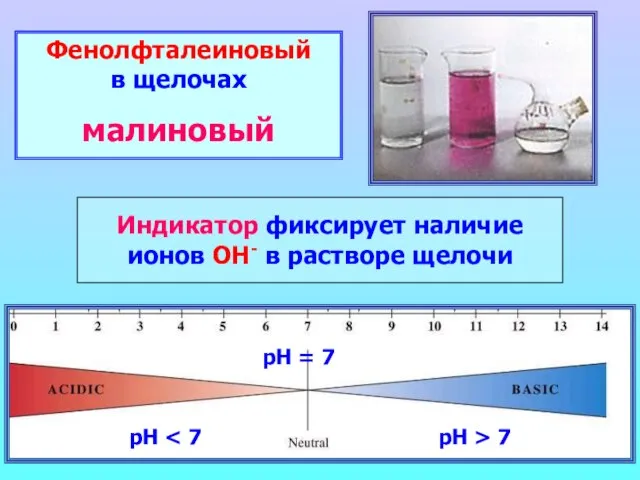
- 9. Фенолфталеиновый в щелочах малиновый Индикатор фиксирует наличие ионов ОН- в растворе щелочи рН рН = 7
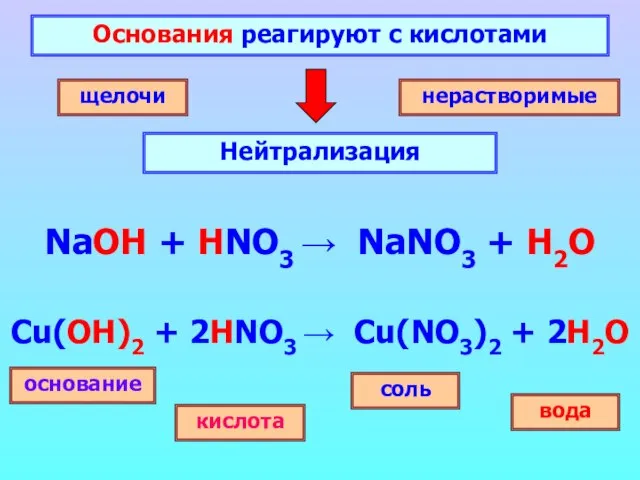
- 10. Основания реагируют с кислотами Нейтрализация щелочи нерастворимые основание соль кислота вода
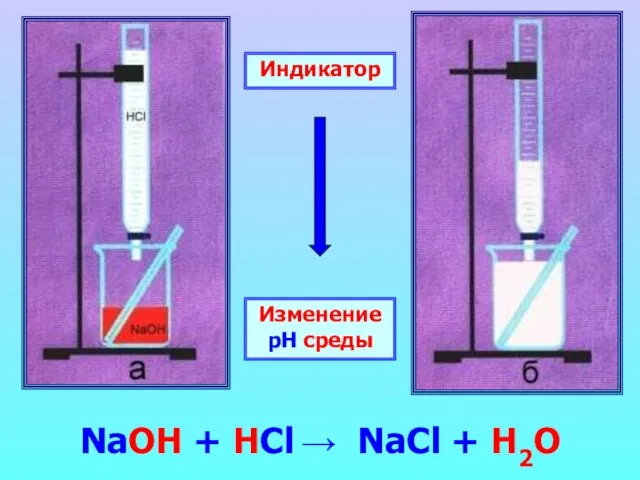
- 12. Индикатор Изменение рН среды
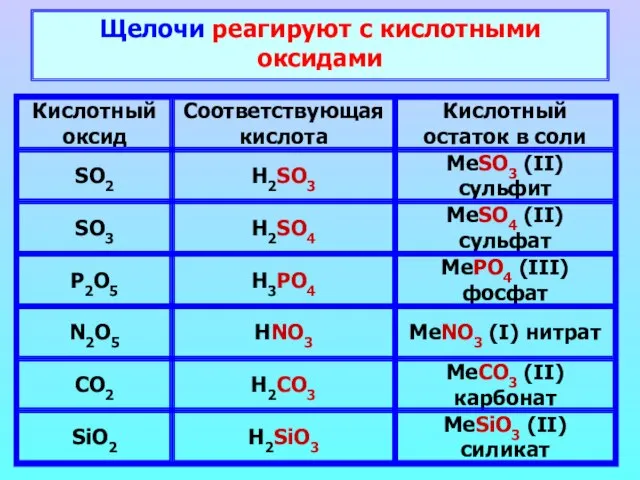
- 13. Щелочи реагируют с кислотными оксидами
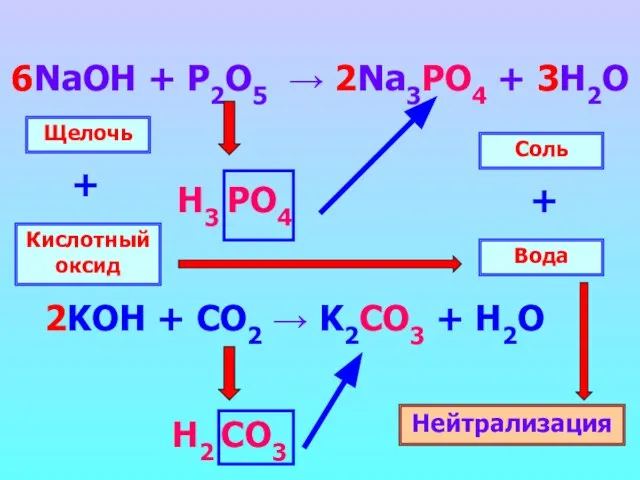
- 14. 6NaOH + P2O5 → 2Na3PO4 + 3H2O Н3 PO4 Н2 CO3 Щелочь Кислотный оксид + Вода
- 15. Нерастворимые основания при нагревании разлагаются 2Fe(OH)3 → Fe2O3 + 3H2O Гидроксид Оксид металла Вода +
- 17. Скачать презентацию



 Формирование и контроль остаточных напряжений, возникающих под действием различных технологических операций
Формирование и контроль остаточных напряжений, возникающих под действием различных технологических операций Особенности строения твердых тел
Особенности строения твердых тел Типы химических реакций
Типы химических реакций Углеводы
Углеводы Презентация по Химии "Лекции по общей и неорганической химии" - скачать смотреть бесплатно
Презентация по Химии "Лекции по общей и неорганической химии" - скачать смотреть бесплатно Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Алканы. Углеводороды. Предельные (насыщенные, алканы)
Алканы. Углеводороды. Предельные (насыщенные, алканы) Биологически важные химические элементы. Неорганические соединения
Биологически важные химические элементы. Неорганические соединения Моделирование (7 класс)
Моделирование (7 класс) ОСНОВАНИЕ
ОСНОВАНИЕ Тема:Хімія
Тема:Хімія  Хиральные производные тиомочевины и скуарамидов в асимметрическом катализе
Хиральные производные тиомочевины и скуарамидов в асимметрическом катализе Получение водорода в промышленности и его применение Химия 8 класс
Получение водорода в промышленности и его применение Химия 8 класс Уксусная кислота (эта́новая кислота)
Уксусная кислота (эта́новая кислота) Fuziunea nucleara
Fuziunea nucleara Многообразие органических веществ
Многообразие органических веществ Презентация по Химии "История спичек" - скачать смотреть
Презентация по Химии "История спичек" - скачать смотреть  Электродные потенциалы
Электродные потенциалы Свойства неметаллов и их соединений. Практическая работа №4
Свойства неметаллов и их соединений. Практическая работа №4 Окислительно - восстановительные реакции
Окислительно - восстановительные реакции Презентация по Химии "Углекислый газ" - скачать смотреть
Презентация по Химии "Углекислый газ" - скачать смотреть  Аттестаионная работа. Сахар. Изучаем и исследуем
Аттестаионная работа. Сахар. Изучаем и исследуем Термический анализ. Прибор синхронного термического анализа
Термический анализ. Прибор синхронного термического анализа История развития технологий термического крекинга в России и мире
История развития технологий термического крекинга в России и мире Побутова хімія У чому її користь, а у чому шкода?
Побутова хімія У чому її користь, а у чому шкода?  Алкан «бутан» (C4H10)
Алкан «бутан» (C4H10) Косметичні засоби Виконала учениця 9 класу Максименко Анастасія
Косметичні засоби Виконала учениця 9 класу Максименко Анастасія  Правило смещения. Радиоактивность. Изотопы
Правило смещения. Радиоактивность. Изотопы