Содержание
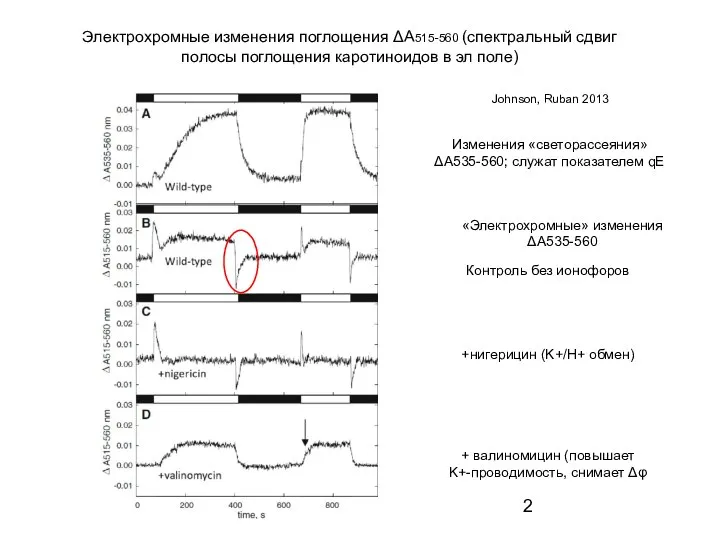
- 2. Электрохромные изменения поглощения ΔА515-560 (спектральный сдвиг полосы поглощения каротиноидов в эл поле) Изменения «светорассеяния» ΔА535-560; служат
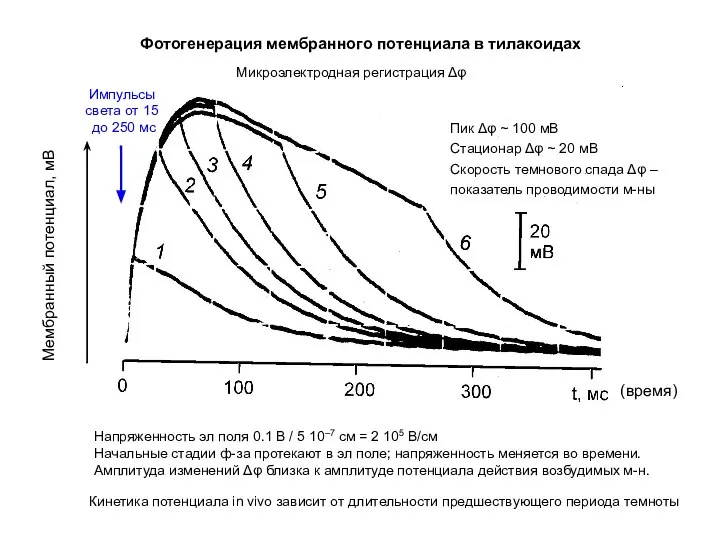
- 3. Фотогенерация мембранного потенциала в тилакоидах Импульсы света от 15 до 250 мс Пик Δφ ~ 100
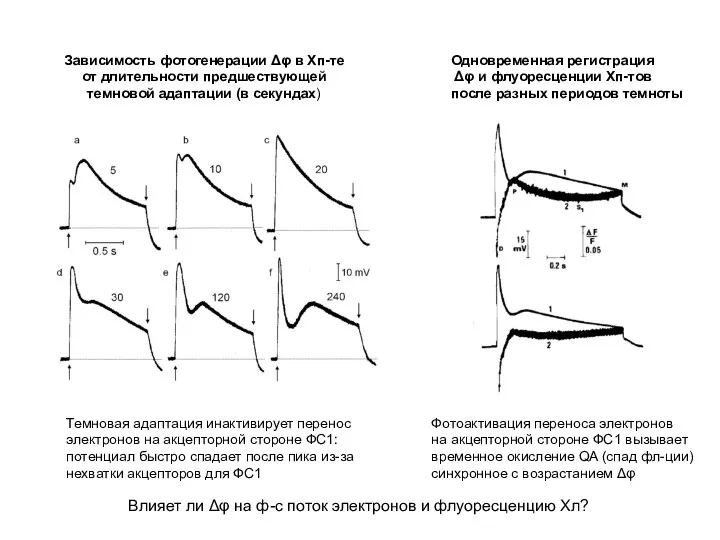
- 4. Зависимость фотогенерации Δφ в Хп-те от длительности предшествующей темновой адаптации (в секундах) Одновременная регистрация Δφ и
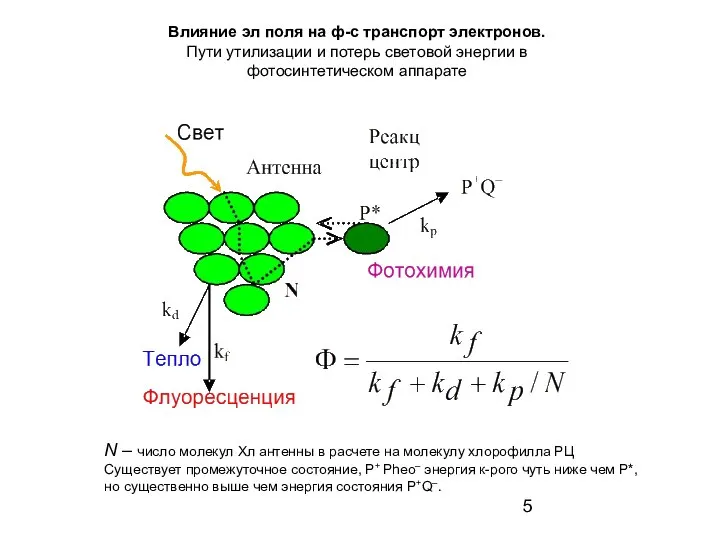
- 5. Влияние эл поля на ф-с транспорт электронов. Пути утилизации и потерь световой энергии в фотосинтетическом аппарате
- 6. + + h d φ1 Влияние эл. поля на перенос заряда в мембранах φ2 a b
- 7. + + h d φ1 Влияние эл. поля на перенос заряда в мембранах φ2 a b
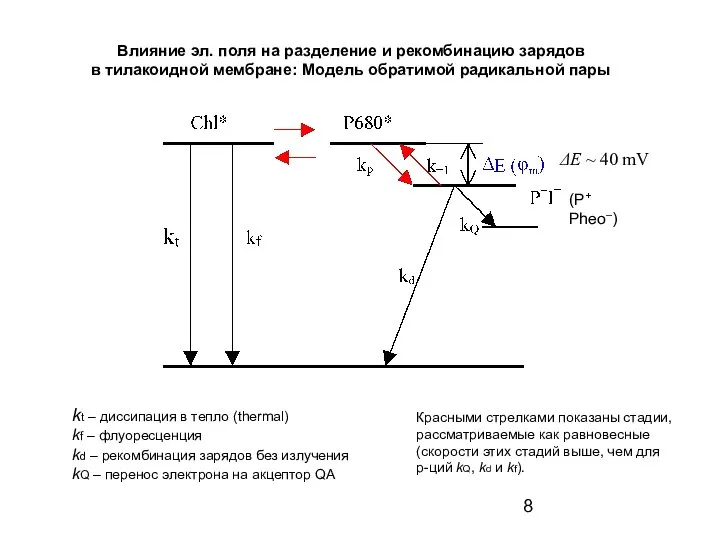
- 8. Влияние эл. поля на разделение и рекомбинацию зарядов в тилакоидной мембране: Модель обратимой радикальной пары kt
- 9. Координата реакции QA окислен QA восстановлен Schatz et al. 1988 [P(Chl)N]* P+I– QA– P+I– Q Есть
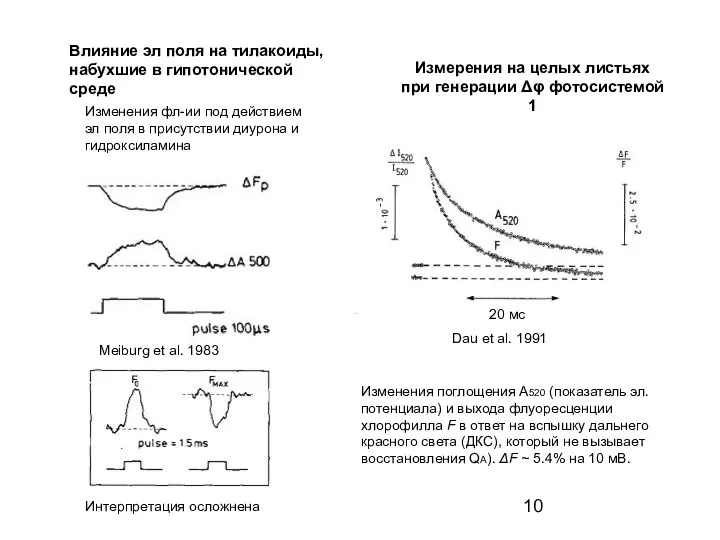
- 10. Влияние эл поля на тилакоиды, набухшие в гипотонической среде Изменения фл-ии под действием эл поля в
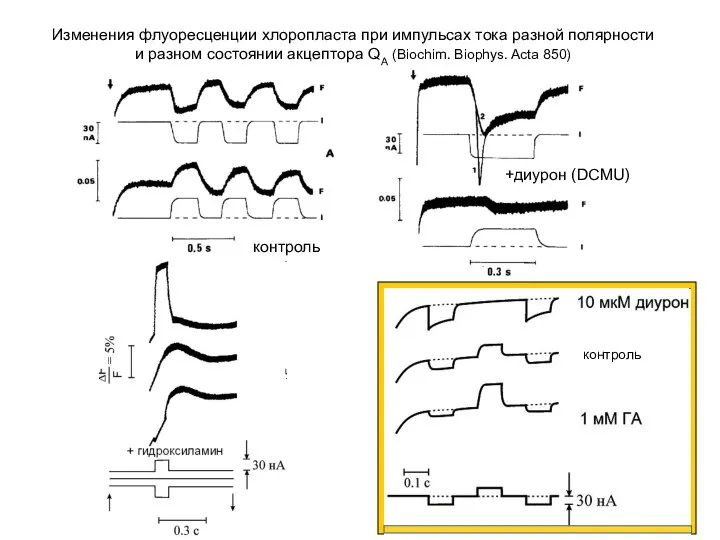
- 11. контроль +диурон (DCMU) Изменения флуоресценции хлоропласта при импульсах тока разной полярности и разном состоянии акцептора QА
- 12. Влияние эл. поля на разделение и рекомбинацию зарядов в тилакоидной мембране Влияние Δφ вызвано изменением отношения
- 13. Влияние потенциала φ на относительную заселенность (вероятность) состояний Р680* и Р+Pheo- (φо – редокс потенциал Р+Pheo-
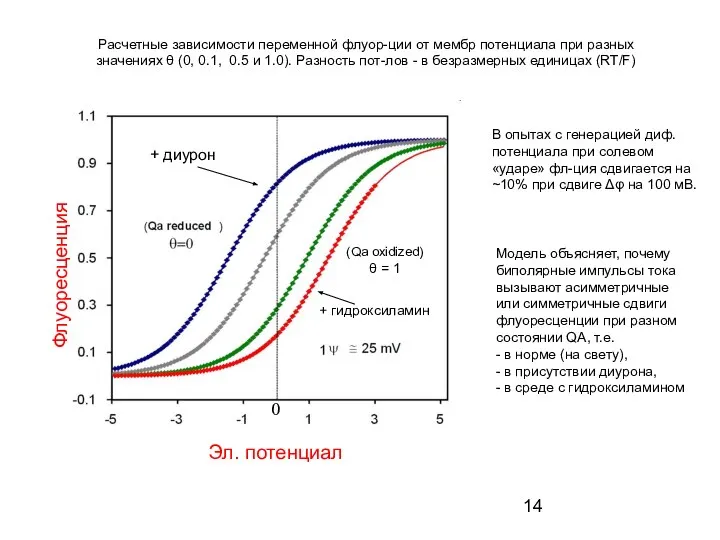
- 14. Эл. потенциал Флуоресценция 0 Расчетные зависимости переменной флуор-ции от мембр потенциала при разных значениях θ (0,
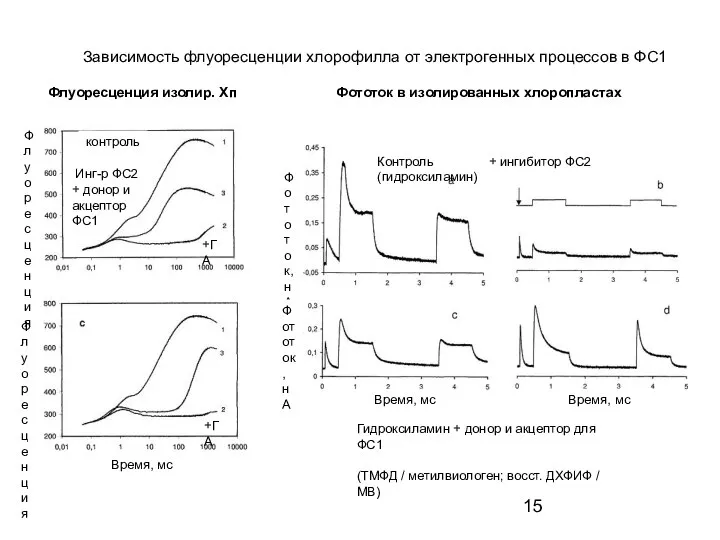
- 15. Зависимость флуоресценции хлорофилла от электрогенных процессов в ФС1 Флуоресценция изолир. Хп Фототок в изолированных хлоропластах контроль
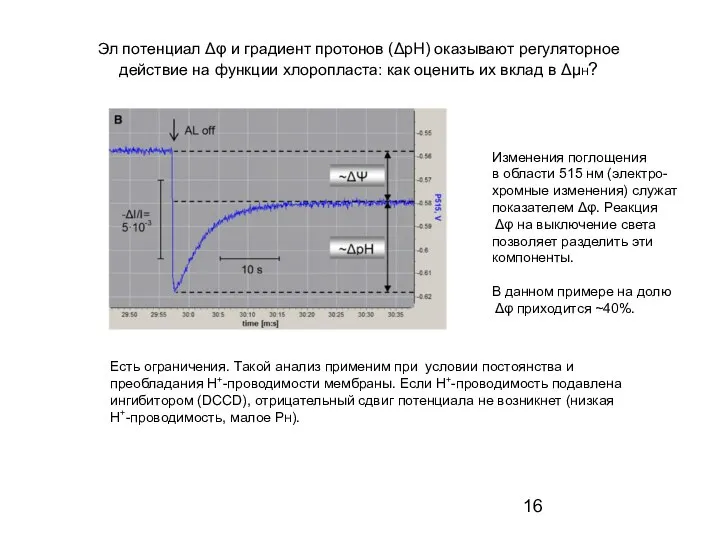
- 16. Эл потенциал Δφ и градиент протонов (ΔрН) оказывают регуляторное действие на функции хлоропласта: как оценить их
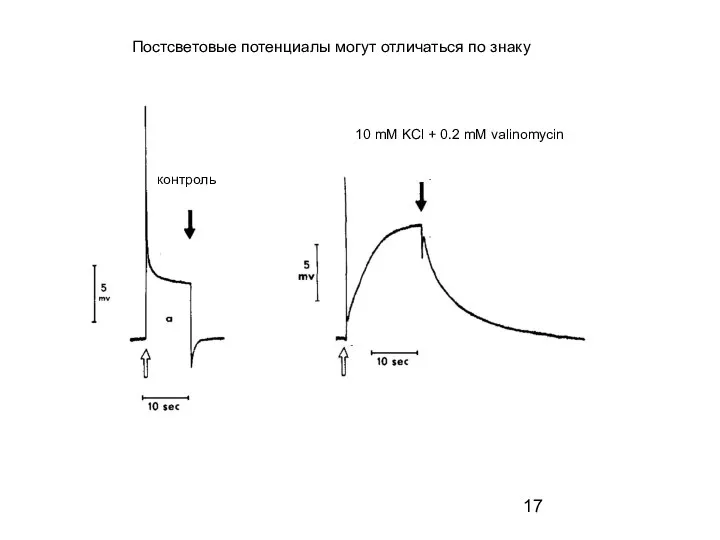
- 17. контроль 10 mM KCl + 0.2 mM valinomycin Постсветовые потенциалы могут отличаться по знаку
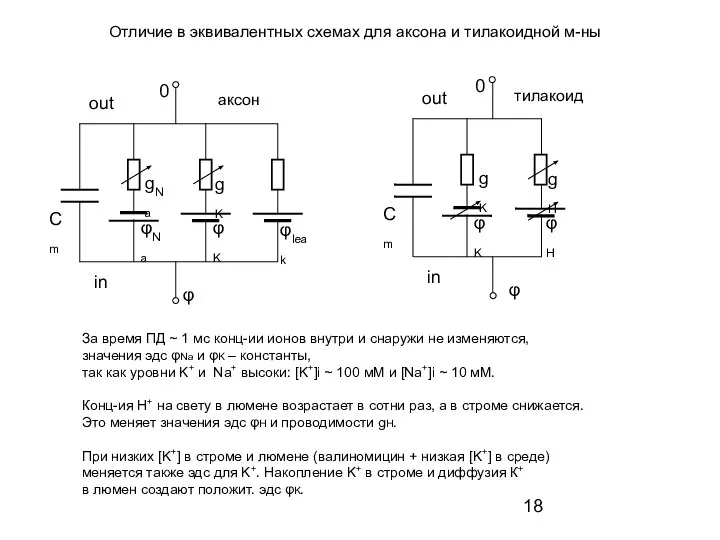
- 18. Сm φK gK φH gH φ 0 in out Отличие в эквивалентных схемах для аксона и
- 20. Скачать презентацию


![Координата реакции QA окислен QA восстановлен Schatz et al. 1988 [P(Chl)N]*](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1395729/slide-8.jpg)


 Химические свойства металлов
Химические свойства металлов Презентация по химии «Соли. Названия и классификация солей»
Презентация по химии «Соли. Названия и классификация солей»  Сплави металів
Сплави металів Аппараты основных химических производств
Аппараты основных химических производств Органическая химия
Органическая химия 11 класс Урок по теме Почему протекают химические реакции Составитель презентации – учитель химии МОУ СОШ им. А.С. Попова Иванова
11 класс Урок по теме Почему протекают химические реакции Составитель презентации – учитель химии МОУ СОШ им. А.С. Попова Иванова  Законы химической термодинамики. Часть 1. Физическая и коллоидная химия
Законы химической термодинамики. Часть 1. Физическая и коллоидная химия Глицерин. Основные способы получения
Глицерин. Основные способы получения Узагальнення знань з теми «Вуглеводні»
Узагальнення знань з теми «Вуглеводні» Коллоидные растворы. Методы получения и очистки коллоидных растворов. Строение мицеллы гидрофобных систем. (Часть 1)
Коллоидные растворы. Методы получения и очистки коллоидных растворов. Строение мицеллы гидрофобных систем. (Часть 1) Охорона довкілля від забруднень при обробці вуглеводневої сировини Підготували учениці 11-А класу Ковальова Анастасія та Лі
Охорона довкілля від забруднень при обробці вуглеводневої сировини Підготували учениці 11-А класу Ковальова Анастасія та Лі Натуральный и синтетический каучуки. Резина
Натуральный и синтетический каучуки. Резина The ideal gas equation
The ideal gas equation Физико-химические основы получения лекарственных препаратов. Классы дисперсных систем
Физико-химические основы получения лекарственных препаратов. Классы дисперсных систем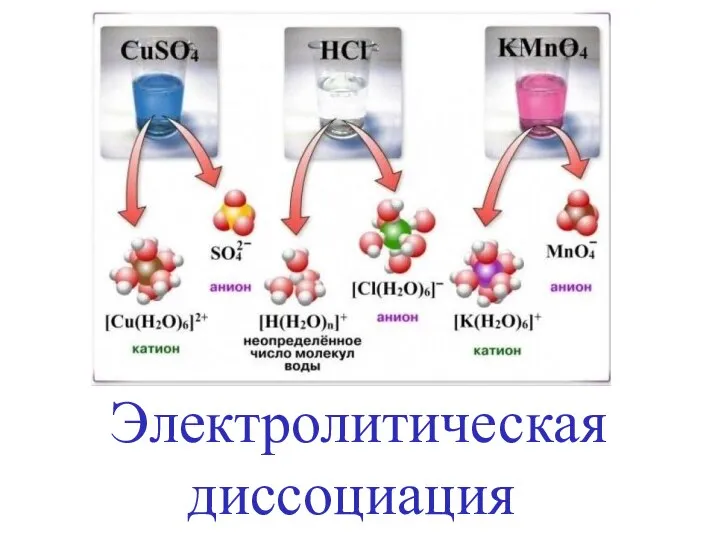 Электролитическая диссоциация
Электролитическая диссоциация Моносахариды, дисахариды
Моносахариды, дисахариды КИСЛОРОД
КИСЛОРОД  Хімічна кінетика
Хімічна кінетика Растворы
Растворы Массообменные процессы
Массообменные процессы Полимеры. Структура и свойства
Полимеры. Структура и свойства Презентация по Химии "Основные химические понятия." - скачать смотреть бесплатно_
Презентация по Химии "Основные химические понятия." - скачать смотреть бесплатно_ Фосфор и его соединения
Фосфор и его соединения Синтез карбамида (лекция 17)
Синтез карбамида (лекция 17) Элементы IV группы, побочной подгруппы периодической системы Менделеева
Элементы IV группы, побочной подгруппы периодической системы Менделеева Утворення кристалів у природі
Утворення кристалів у природі  Биологически важные реакции монофункциональных соединений. Реакционная способность спиртов, фенолов, тиолов, аминов
Биологически важные реакции монофункциональных соединений. Реакционная способность спиртов, фенолов, тиолов, аминов Современные способы защиты ОТТ
Современные способы защиты ОТТ