Содержание
- 2. План лекции 1. Сущность периодического закона. Причина периодической повторяемости химических свойств и количественных характеристик атомов с
- 3. 3 п.1. Сущность периодического закона. Причина периодической повторяемости химических свойств и количественных характеристик атомов с увеличением
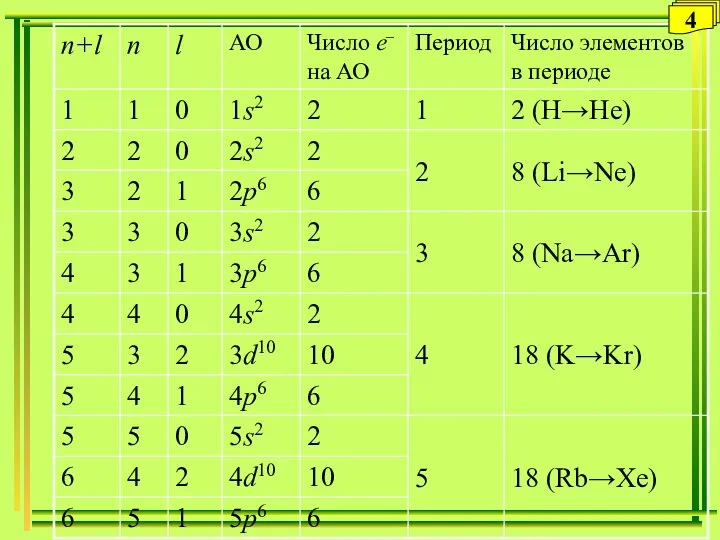
- 4. 4
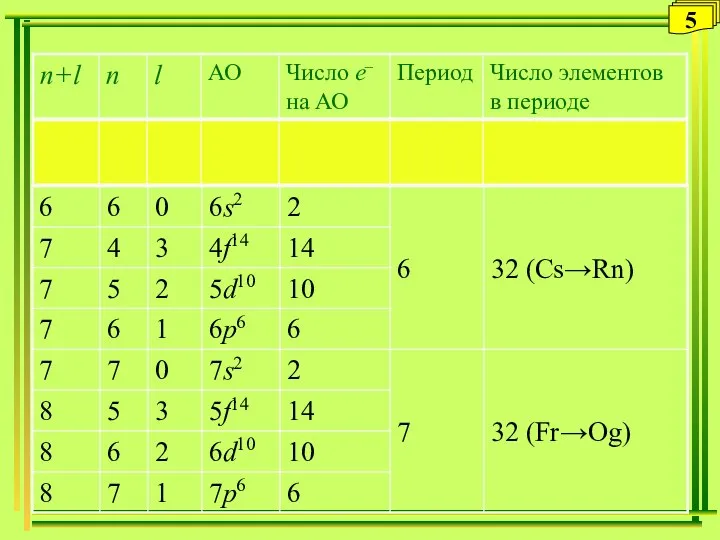
- 5. 5
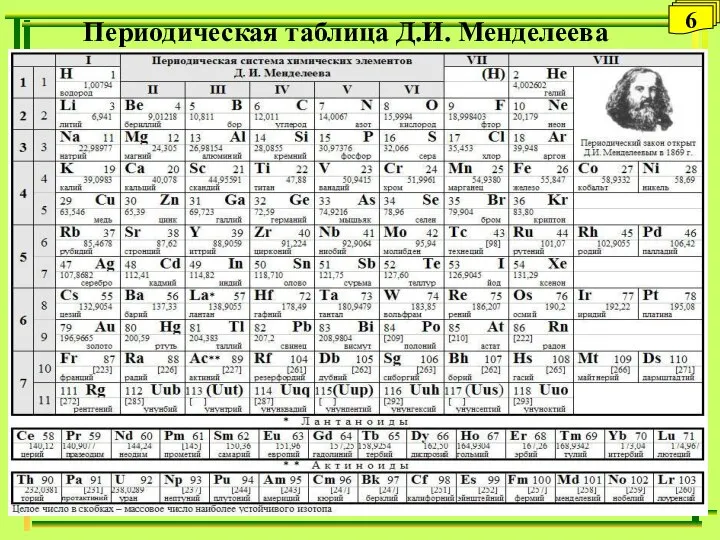
- 6. Периодическая таблица Д.И. Менделеева 6
- 7. 7
- 8. Периодический закон "Свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости
- 9. Периодический закон сегодня: "Свойства химических элементов, а также образуемых ими простых и сложных веществ находятся в
- 10. Периодическая система химических элементов Периодическая система химических элементов - естественная классификация химических элементов, являющаяся табличным выражением
- 11. Периодичность Периодичность – это повторяемость химических и физических свойств элементов и их соединений по определенному направлению
- 12. 12 п.2. Строение периодической системы химических элементов Д.И. Менделеева. Характер и причины изменения металлических и неметаллических
- 13. Энергия ионизации Энергия (потенциал) ионизации атома Ei - минимальная энергия, необходимая для удаления электрона из атома:
- 14. Сродство к электрону Сродство атома к электрону Ee – способность атомов присоединять добавочный электрон и превращаться
- 15. Электроотрицательность (абсолютная электроотрицательность) Относительная электроотрицательность: χLi = 1 χF = 4 Лайнус-Карл ПОЛИНГ (28.02.1901 – 19.08.1994)
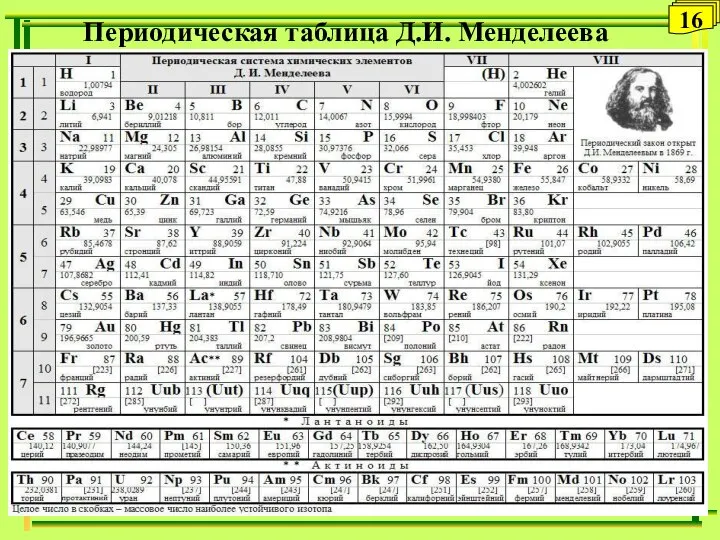
- 16. Периодическая таблица Д.И. Менделеева 16
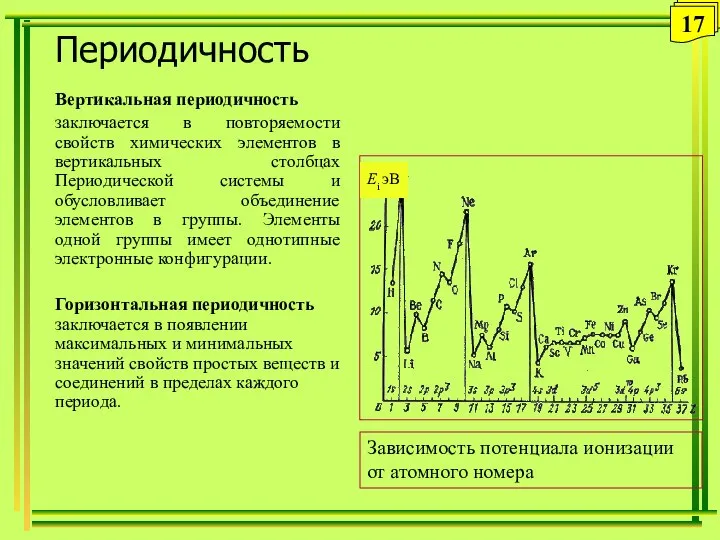
- 17. Периодичность Вертикальная периодичность заключается в повторяемости свойств химических элементов в вертикальных столбцах Периодической системы и обусловливает
- 18. П.3 Электронные s-,p-,d и f- семейства это связь между положением элемента в периодической системе и электронным
- 19. п.3. Основные типы химической связи (ковалентная, ионная, металлическая, водородная), механизм их образования и свойства. Под химической
- 20. Ковалентная химическая связь это связь, возникающая между атомами за счет образования общих электронных пар 20 Параметры
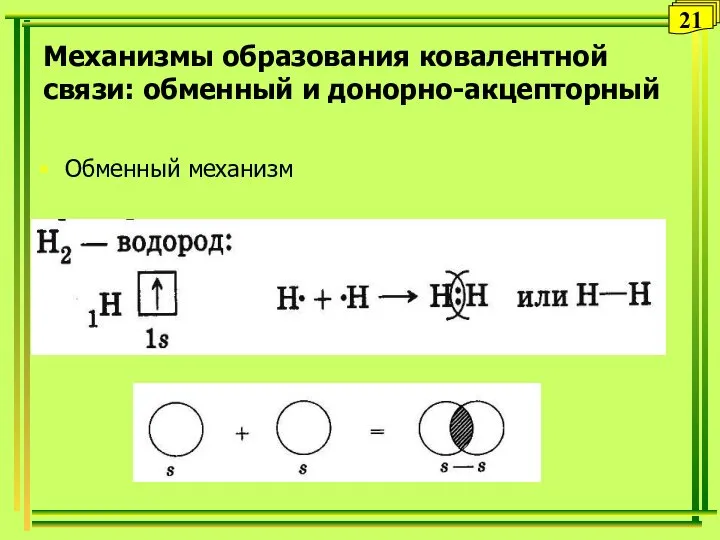
- 21. Обменный механизм 21 Механизмы образования ковалентной связи: обменный и донорно-акцепторный
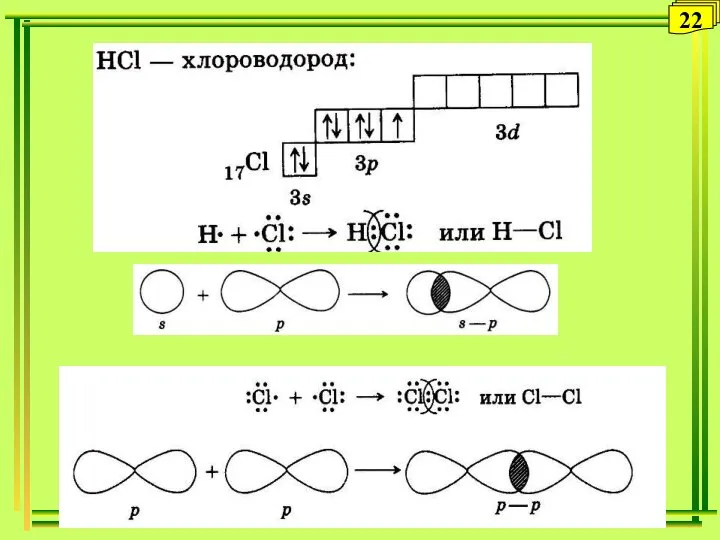
- 22. 22
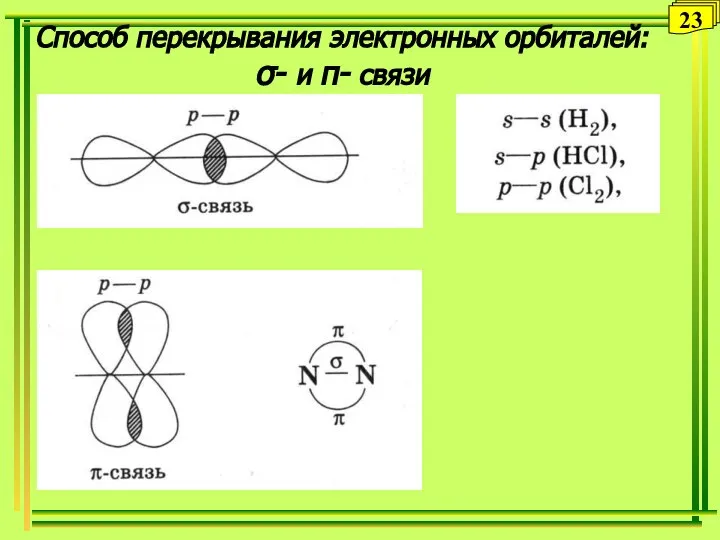
- 23. Способ перекрывания электронных орбиталей: σ- и π- связи 23
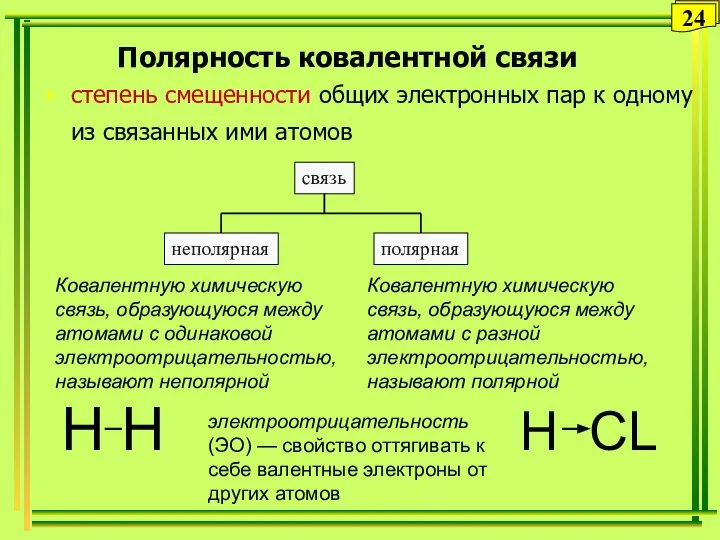
- 24. Полярность ковалентной связи степень смещенности общих электронных пар к одному из связанных ими атомов электроотрицательность (ЭО)
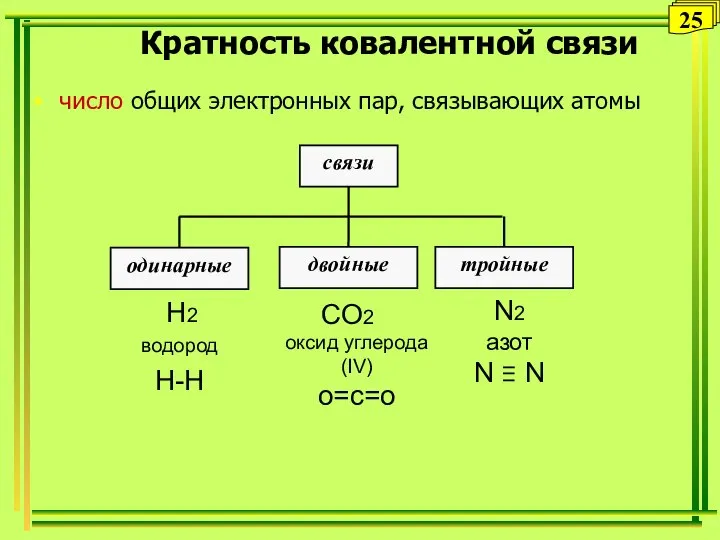
- 25. Кратность ковалентной связи число общих электронных пар, связывающих атомы 25
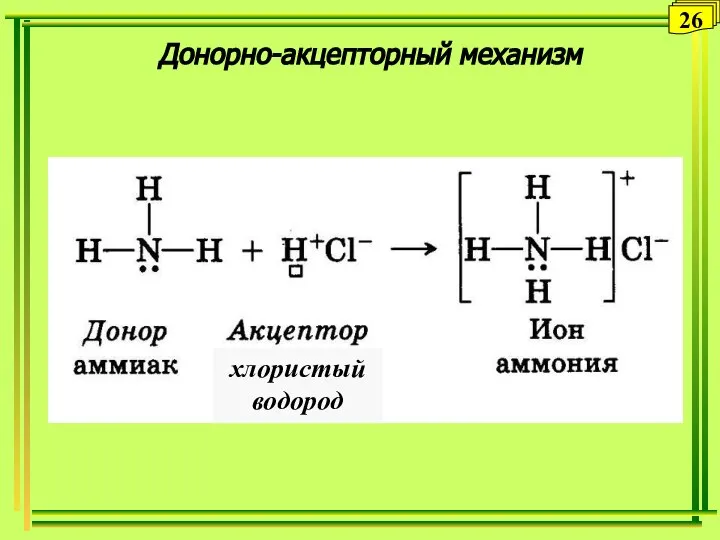
- 26. Донорно-акцепторный механизм 26
- 27. Гибридизация атомных орбиталей Гибридизация – это выравнивание (усреднение) энергетических и геометрических характеристик атомных орбиталей разных подуровней
- 28. Примеры гибридизации (sp) 4Be: [He]2s2 4Be*: [He]2s12p1 s-АО + p-АО = 2sp-АО 28
- 29. Примеры гибридизации (sp2) 5B: [He]2s22p1 5B*: [He]2s12p2 s-АО + 2p-АО = 3sp2-АО Плоский треугольник 29
- 30. Примеры гибридизации (sp3) 6С: [He]2s22p2 6С*: [He]2s12p3 s-АО + 3p-АО = 4sp3-АО Тетраэдр 30
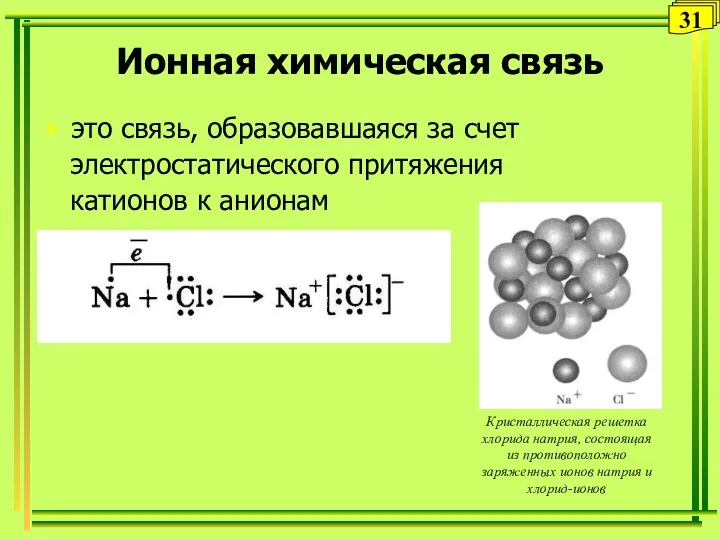
- 31. Ионная химическая связь это связь, образовавшаяся за счет электростатического притяжения катионов к анионам 31 Кристаллическая решетка
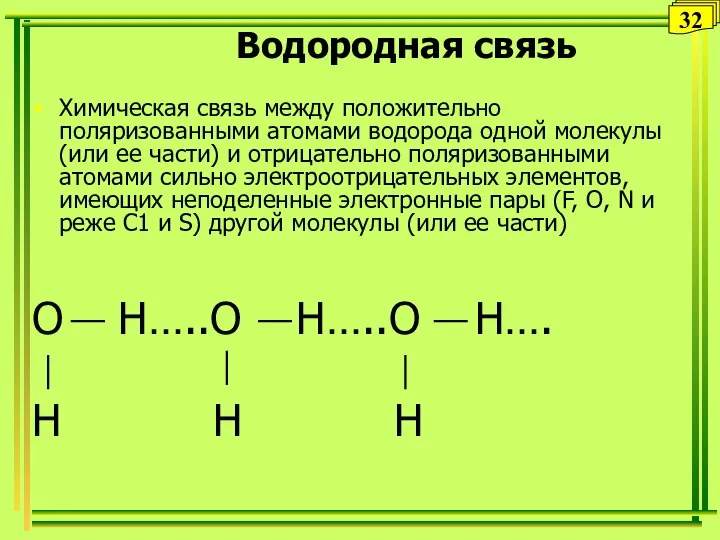
- 32. Водородная связь Химическая связь между положительно поляризованными атомами водорода одной молекулы (или ее части) и отрицательно
- 33. Металлическая связь связь в металлах и сплавах, которую выполняют относительно свободные электроны между ионами металлов в
- 34. 34 Вопросы к экзамену по общей и неорганической химии 1. Понятия: материя, вещество. Предмет науки химия
- 36. Скачать презентацию















![Примеры гибридизации (sp) 4Be: [He]2s2 4Be*: [He]2s12p1 s-АО + p-АО = 2sp-АО 28](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1401777/slide-27.jpg)
![Примеры гибридизации (sp2) 5B: [He]2s22p1 5B*: [He]2s12p2 s-АО + 2p-АО = 3sp2-АО Плоский треугольник 29](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1401777/slide-28.jpg)
![Примеры гибридизации (sp3) 6С: [He]2s22p2 6С*: [He]2s12p3 s-АО + 3p-АО = 4sp3-АО Тетраэдр 30](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1401777/slide-29.jpg)


 Кристалічні та аморфні тіла. Рідкі кристали та їх властивості
Кристалічні та аморфні тіла. Рідкі кристали та їх властивості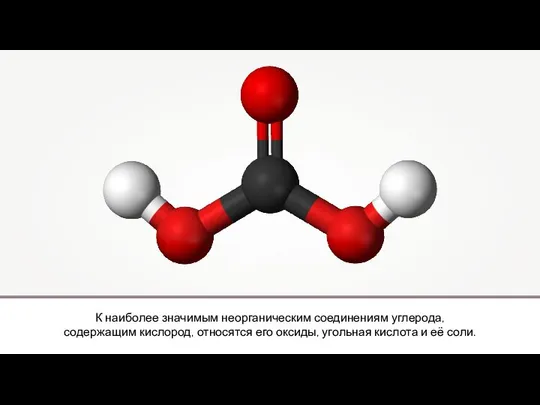 Кислородные соединения углерода
Кислородные соединения углерода Нефть. Состав нефти
Нефть. Состав нефти Особенности познания в химии
Особенности познания в химии Аминокислоты «Единственный путь, ведущий к знанию – это деятельность» Б. Шоу
Аминокислоты «Единственный путь, ведущий к знанию – это деятельность» Б. Шоу Презентация по Химии "Соли в медицине" - скачать смотреть
Презентация по Химии "Соли в медицине" - скачать смотреть  Дисахариды и полисахариды
Дисахариды и полисахариды Презентация по Химии "Всё о соли" - скачать смотреть
Презентация по Химии "Всё о соли" - скачать смотреть  Аттестационная работа. Образовательная программа внеурочной деятельности Химия красок
Аттестационная работа. Образовательная программа внеурочной деятельности Химия красок Применение неметаллов и их соединений
Применение неметаллов и их соединений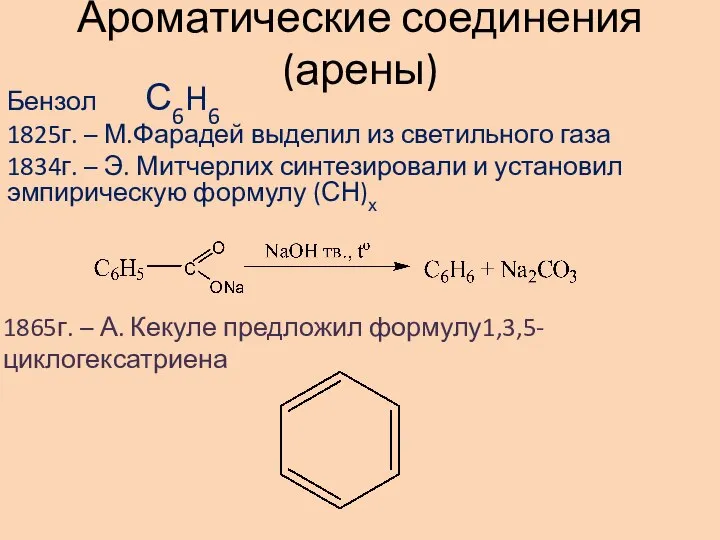 Ароматические соединения (арены)
Ароматические соединения (арены) Типы химической связи
Типы химической связи Алмаз
Алмаз Физическая химия тугоплавких неметаллических и силикатных материалов. Дисперсные системы. (Лекции 1-3)
Физическая химия тугоплавких неметаллических и силикатных материалов. Дисперсные системы. (Лекции 1-3) Основные классы неорганических соединений
Основные классы неорганических соединений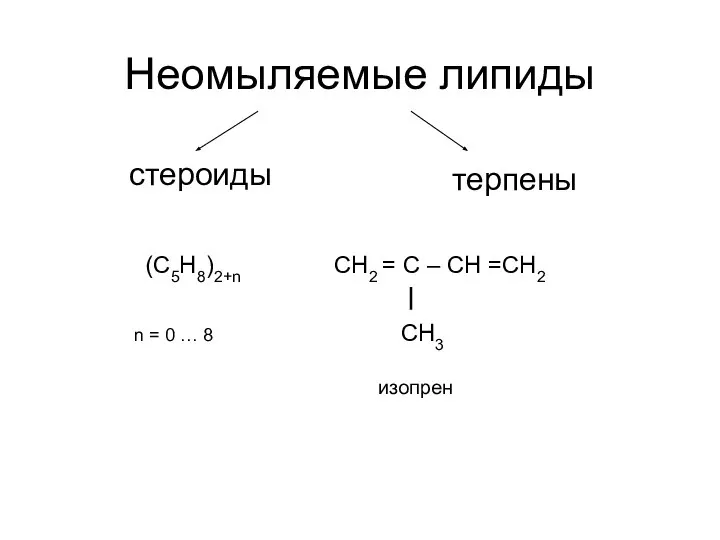 Неомыляемые липиды. Стероиды
Неомыляемые липиды. Стероиды Равновесие в растворах электролитов
Равновесие в растворах электролитов Физико-химические свойства крахмала
Физико-химические свойства крахмала Химия и стирка
Химия и стирка  Allgemeine Chemie für PharmazeutInnen
Allgemeine Chemie für PharmazeutInnen Поверхностное упрочнение деталей. (Лекция 11)
Поверхностное упрочнение деталей. (Лекция 11) Определение активности ферментов
Определение активности ферментов Дослідження на тему: Історія назви міста За проектом “Екологічна ситуація у рідному місті”
Дослідження на тему: Історія назви міста За проектом “Екологічна ситуація у рідному місті” Химия вокруг нас
Химия вокруг нас Оксиды. Номенклатура, классификация, физические свойства
Оксиды. Номенклатура, классификация, физические свойства Количественное определение лекарственных веществ
Количественное определение лекарственных веществ Ағзалар мен биосұйықтар минерализатындағы металдық улар
Ағзалар мен биосұйықтар минерализатындағы металдық улар Классификация металлов
Классификация металлов