Содержание
- 2. Комплексные соединения: история открытия и изучения
- 3. История открытия и изучения Одним из первых описанных соединений такого типа были желтая и красная кровяные
- 4. Теория Вернера: термины Комплексообразователь (центральный атом) – ион или нейтральный атом металла со свободными электронными ячейками;
- 5. Образование комплексной частицы Связи между ЦА и лигандами могут быть как электростатическими, так и обр. по
- 6. Изомерия комплексов Пространственная: цис- и транс-, ос- и гран- изомеры. Оптическая изомерия Гидратная изомерия Ионазиционная Координационная
- 7. Номенклатура комплексных соединений Лиганды перечисляются в последовательности от отрицательных (с добавлением -о) к нейтральным и положительным;
- 8. Реакции комплексных соединений Вступают в реакции: Обмена ионами внешней сферы; Обмена лигандами; Окисления (ЦА); Разрушения и
- 9. Примеры реакций комплексных соединений
- 10. Разрушение и получение аквакомплексов При нагревании твердых кристаллогидратов аквакомплекс рушится и изменяется цвет солей: CuSO4*5H2O =
- 11. Получение гидроксокомплексов Соли амфотерных металлов способны давать растворимые комплексы в избытке щелочи: Al3+ + 6 OH-
- 12. Получение аммиакатов Многие металлы образуют комплексные соединения с аммиаком. Al3+, Pb2+ - не дают аммиакатов! Zn2+
- 13. Цианоферратные комплексы Получение «берлинской лазури» или «турнбулевой сини»: Fe2+ + K3[Fe(CN)6] = KFe[Fe(CN)6] + 2K+ Fe3+
- 14. Образование роданидных комплексов Роданид-анион способен к образованию прочных соединений с ионами кобальта-II и железа-III: Fe3+ +
- 15. Разрушение роданидных комплексов Довольно прочный комплекс железа разрушается фторид-ионами: [Fe(NCS)3] + 6 NaFтв. = Na3[FeF6] +
- 16. Качественная реакция на енолы Для качественного определения енолов используют соли Fe3+, дающие окрашенный комплекс. фенол аскорбиновая
- 17. Комплексы с ДМГО Качественная специфичная реакция на Ni2+ с диметилглиоксимом (ДМГО) – реактивом Чугаева. Подобную реакцию
- 18. Получение хлоридного комплекса меди-II Гидрат-ион меди-II способен замещать воду в КС на хлорид-ионы при высокой их
- 19. Получение гликолята меди-II Ион меди-II способен реагировать в сильнощелочной среде с гликолями (вицинальными диолами), например –
- 20. Биуретовая реакция (на амидные группы) Ион меди-II в щелочном растворе белка координируется 4 азотами амидных групп
- 21. Качественная реакция на ион калия Для определения она калия в растворе используют кобальтинитрит натрия: 3 K+
- 22. Качественная реакция на кислород Соединения меди-I неустойчивы на воздухе и легко окисляются кислородом воздуха. На окислении
- 23. Получение надхромовой кислоты Соединения Cr +6 могут образовывать надхромовую кислоту в реакциях с перекисью водорода. Эта
- 25. Скачать презентацию











![Цианоферратные комплексы Получение «берлинской лазури» или «турнбулевой сини»: Fe2+ + K3[Fe(CN)6]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1392605/slide-12.jpg)

![Разрушение роданидных комплексов Довольно прочный комплекс железа разрушается фторид-ионами: [Fe(NCS)3] +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1392605/slide-14.jpg)








 Кристалічні та аморфні тіла. Рідкі кристали та їх властивості
Кристалічні та аморфні тіла. Рідкі кристали та їх властивості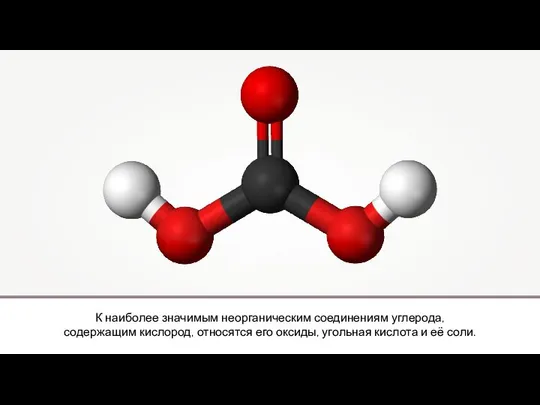 Кислородные соединения углерода
Кислородные соединения углерода Нефть. Состав нефти
Нефть. Состав нефти Особенности познания в химии
Особенности познания в химии Аминокислоты «Единственный путь, ведущий к знанию – это деятельность» Б. Шоу
Аминокислоты «Единственный путь, ведущий к знанию – это деятельность» Б. Шоу Презентация по Химии "Соли в медицине" - скачать смотреть
Презентация по Химии "Соли в медицине" - скачать смотреть  Дисахариды и полисахариды
Дисахариды и полисахариды Презентация по Химии "Всё о соли" - скачать смотреть
Презентация по Химии "Всё о соли" - скачать смотреть  Аттестационная работа. Образовательная программа внеурочной деятельности Химия красок
Аттестационная работа. Образовательная программа внеурочной деятельности Химия красок Применение неметаллов и их соединений
Применение неметаллов и их соединений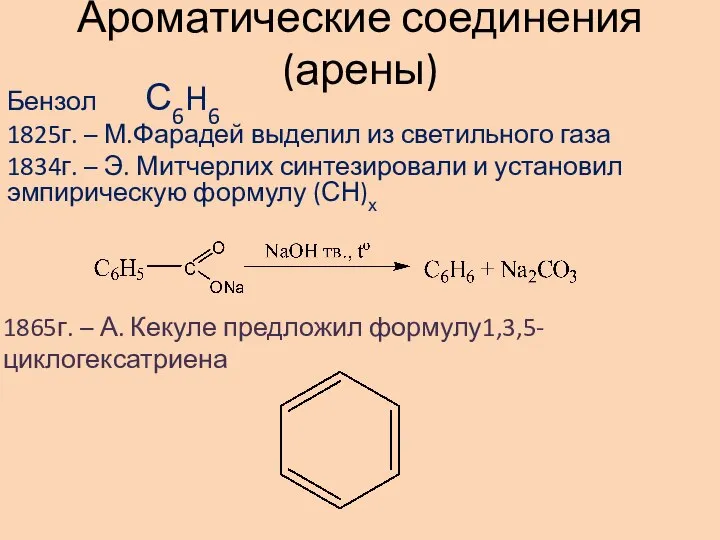 Ароматические соединения (арены)
Ароматические соединения (арены) Типы химической связи
Типы химической связи Алмаз
Алмаз Физическая химия тугоплавких неметаллических и силикатных материалов. Дисперсные системы. (Лекции 1-3)
Физическая химия тугоплавких неметаллических и силикатных материалов. Дисперсные системы. (Лекции 1-3) Основные классы неорганических соединений
Основные классы неорганических соединений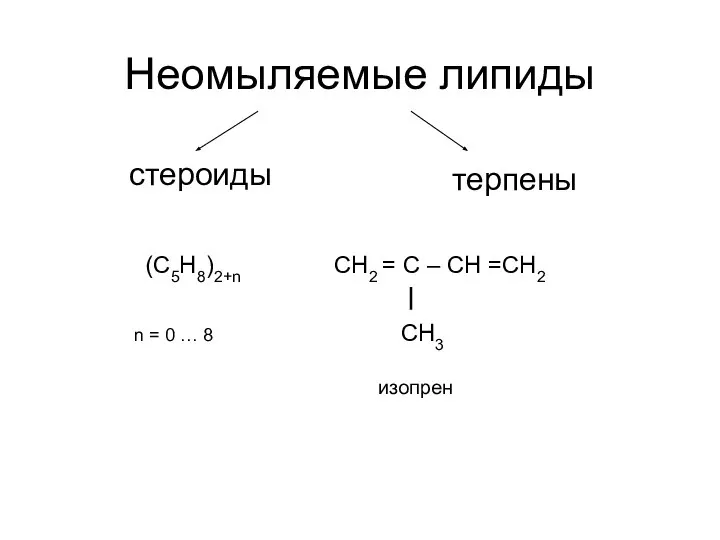 Неомыляемые липиды. Стероиды
Неомыляемые липиды. Стероиды Равновесие в растворах электролитов
Равновесие в растворах электролитов Физико-химические свойства крахмала
Физико-химические свойства крахмала Химия и стирка
Химия и стирка  Allgemeine Chemie für PharmazeutInnen
Allgemeine Chemie für PharmazeutInnen Поверхностное упрочнение деталей. (Лекция 11)
Поверхностное упрочнение деталей. (Лекция 11) Определение активности ферментов
Определение активности ферментов Дослідження на тему: Історія назви міста За проектом “Екологічна ситуація у рідному місті”
Дослідження на тему: Історія назви міста За проектом “Екологічна ситуація у рідному місті” Химия вокруг нас
Химия вокруг нас Оксиды. Номенклатура, классификация, физические свойства
Оксиды. Номенклатура, классификация, физические свойства Количественное определение лекарственных веществ
Количественное определение лекарственных веществ Ағзалар мен биосұйықтар минерализатындағы металдық улар
Ағзалар мен биосұйықтар минерализатындағы металдық улар Классификация металлов
Классификация металлов