Содержание
- 2. Закон Гесса.
- 3. Применение закона Гесса Метод термохимических уравнений Метод термохимических схем Метод термохимических уравнений
- 4. Метод термохимических схем ΔН1 ΔН2 ΔН3 +О2 +1/2 О2 +1/2 О2 ΔН2 = -110,53 кДж/моль ΔН3
- 5. Следствия из закона Гесса.
- 7. Зависимость тепловых эффектов химических реакций от температуры. Теплоемкость. Уравнение Кирхгофа.
- 8. Расчеты тепловых эффектов реакций на основе следствий из закона Гесса с использованием справочных термодинамических данных ограничены
- 9. Средние теплоемкости измеряются на определенном интервале температур Истинные теплоемкости соответствуют бесконечно малому изменению температуры Изобарная теплоемкость
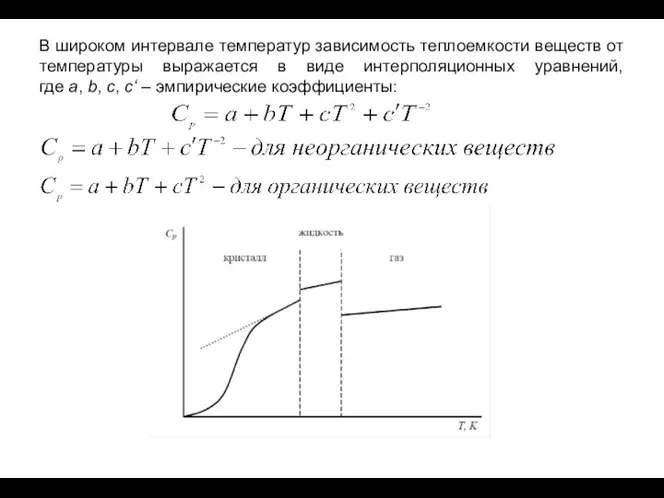
- 10. В широком интервале температур зависимость теплоемкости веществ от температуры выражается в виде интерполяционных уравнений, где a,
- 11. Уравнение Кирхгофа и его интегрирование
- 12. На практике интегрирование обычно проводят от стандартной температуры 298 К до заданной Т, при которой протекает
- 17. 3) При наличии фазовых превращений реагентов на заданном интервале температур
- 18. Процессы: изобарное нагревание твердого вещества от 298К до ТПЛ плавление твердого вещества при ТПЛ изобарное нагревание
- 19. МВЗ № 4 , гл. «Первое начало термодинамики»
- 22. В задаче рассматриваются три метода расчета изменения теплоемкости в химической реакции как функции температуры, которые при
- 28. Скачать презентацию
























 Переосаждение. (Глава 4. § 20. Задача 13)
Переосаждение. (Глава 4. § 20. Задача 13) Геометрия молекул
Геометрия молекул Силикатная промышленность
Силикатная промышленность Галогены
Галогены Валентность
Валентность Главная подгруппа IV группы
Главная подгруппа IV группы Основные понятия и законы химии
Основные понятия и законы химии Строение, свойства, биологическая роль липидов. (Лекция 12)
Строение, свойства, биологическая роль липидов. (Лекция 12) Общая формула алкадиенов
Общая формула алкадиенов Aluminium
Aluminium Хром және оның қосылыстары
Хром және оның қосылыстары Общие химические свойства металлов
Общие химические свойства металлов принцип работы, применение в технике и быту
принцип работы, применение в технике и быту Гідроліз солей
Гідроліз солей Влияние вида основы на качество эмульсионной мази с калия йодидом при изготовлении в аптеке
Влияние вида основы на качество эмульсионной мази с калия йодидом при изготовлении в аптеке Исследование минералов в параллельном свете с одним поляризатором
Исследование минералов в параллельном свете с одним поляризатором Основные законы и понятия химии. Тема №10
Основные законы и понятия химии. Тема №10 Сера и её свойства
Сера и её свойства  Периодический закон и ПСХЭ Д.И. Менделеева в свете учения о строении атома
Периодический закон и ПСХЭ Д.И. Менделеева в свете учения о строении атома Synthesis of Paclitaxel
Synthesis of Paclitaxel Электролиз воды
Электролиз воды Решение задач. Подготовка к контрольной работе по химии
Решение задач. Подготовка к контрольной работе по химии G12 - класс антифризов
G12 - класс антифризов Лучший способ избавиться от искушения – поддаться ему Оскар Уайльд
Лучший способ избавиться от искушения – поддаться ему Оскар Уайльд Кислотно-основні рівноваги в біологічних системах. (Лекція 2)
Кислотно-основні рівноваги в біологічних системах. (Лекція 2) Почвенный раствор. Химический состав почвенных растворов. Водный режим почв. Кислотность и щелочность почвенных растворов
Почвенный раствор. Химический состав почвенных растворов. Водный режим почв. Кислотность и щелочность почвенных растворов Протолитические равновесия в растворах электролитах
Протолитические равновесия в растворах электролитах Характеристика химического элемента
Характеристика химического элемента