Содержание
- 2. 1. Определение Химическая кинетика – раздел химии, изучающий скорость и механизмы химических превращений. Скоростью химической реакции
- 3. 1. Определение Различают среднюю и мгновенную скорость реакции. Средняя скорость реакции определяется отношением изменения концентраций реагирующих
- 4. 1. Определение Скорость всегда положительна. Знак «+» учитывает увеличение концентрации продуктов реакции. Знак «-» ставится в
- 5. 1. Определение Мгновенная (истинная) скорость определяется первой производной концентрации во времени: , при этом учитывается изменение
- 6. 1. Определение Скорость реакции зависит от: Природы реагирующих веществ Концентрации реагирующих веществ Температуры Присутствия катализатора
- 7. 2. Влияние концентрации реагирующих веществ на скорость хим. реакций Влияние концентрации реагирующих веществ на скорость химических
- 8. 2. Влияние концентрации реагирующих веществ на скорость хим. реакций Эта зависимость определяется кинетическим уравнением. Для реакции:
- 9. 2. Влияние концентрации реагирующих веществ на скорость хим. реакций Примерами кинетических уравнений для гомогенных и гетерогенных
- 10. 3. Кинетическая классификация химических реакций Кинетическая классификация химических реакций Кинетические реакции могут быть классифицированы: по молекулярности
- 11. 3. Кинетическая классификация химических реакций По молекулярности различают реакции: мономолекулярные К ним относят реакции разложения, диссоциации,
- 12. 3. Кинетическая классификация химических реакций бимолекулярные Например, реакция взаимодействия водорода и хлора: Вероятность одновременного столкновения многих
- 13. 3. Кинетическая классификация химических реакций Порядок реакции определяется кинетическим уравнением и равен сумме показателей степеней при
- 14. 3. Кинетическая классификация химических реакций а) Нулевой порядок наблюдается в гетерогенных реакциях, в которых велика концентрация
- 15. 3. Кинетическая классификация химических реакций б) Для реакций первого порядка скорость зависит от концентрации только одного
- 16. Кинетическая классификация химических реакций. Молекулярность. Порядок реакции. в) К реакциям второго порядка относятся реакции соединения и
- 17. 3. Кинетическая классификация химических реакций. - показатели порядка реакции по реагентам А и В - суммарный
- 18. 3. Кинетическая классификация химических реакций Для сложных многостадийных реакций и могут быть определены только экспериментально. Обычно
- 19. г) дробный порядок наблюдается в случаях, если: химическая реакция протекает в несколько стадий реагирующие вещества резко
- 20. 3. Кинетическая классификация химических реакций. Рассмотрим реакцию хлорирования тетрахлороэтилена с образованием гексахлороэтана: Данная реакция является бимолекулярной,
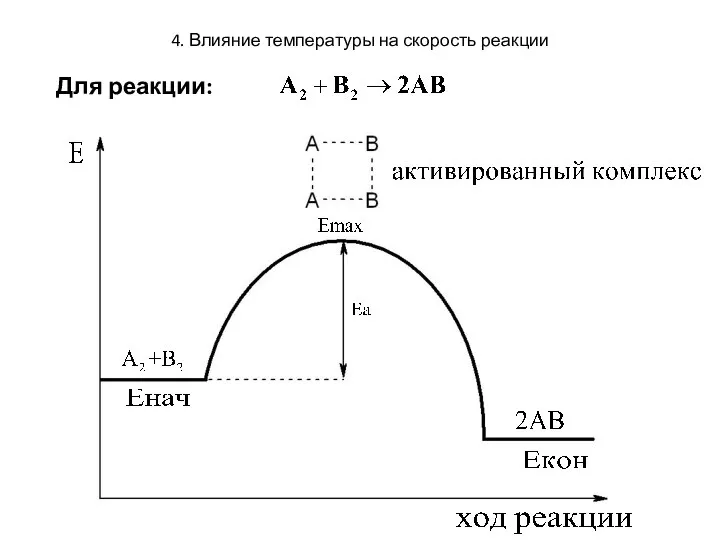
- 21. 4. Влияние температуры на скорость реакции Влияние температуры на скорость реакции. Энергия активации. В системе химического
- 22. 4. Влияние температуры на скорость реакции Активированный комплекс существует очень короткое время (10-13 сек) , его
- 23. 4. Влияние температуры на скорость реакции Для реакции:
- 24. 4. Влияние температуры на скорость реакции Преодолеть энергетический барьер способны лишь так называемые активные частицы –
- 25. 4. Влияние температуры на скорость реакции С точки зрения теории активации скорость реакции можно увеличить двумя
- 26. 4. Влияние температуры на скорость реакции Зависимость скорости реакции от температуры и энергии активации определяется уравнением
- 27. 4. Влияние температуры на скорость реакции Если Еа = 84 – 170 КДж∙моль-1 (что характерно для
- 28. 4. Влияние температуры на скорость реакции t1 – начальная температура t2 – конечная температура – скорости
- 29. 4. Влияние температуры на скорость реакции Для большинства биохимических реакций =2 – 4 но некоторые ферментативные
- 30. 5. Катализ Катализ Катализом называется селективное изменение скорости химической реакции веществом, которое участвует в реакции, но
- 31. 5. Катализ Действие катализатора основано на образовании между ним и компонентами реакции промежуточных соединений, энергия активации
- 32. 5. Катализ По механизму действия различают: 1. гомогенный катализ 2. гетерогенный катализ 3. ферментативный катализ Общим
- 33. 5. Катализ 3. Катализаторы не влияют на величину констант равновесия. 4.Катализаторы чувствительны к наличию посторонних веществ.
- 34. 5. Катализ Ферментативный катализ Ферменты (энзимы) – биологические катализаторы, вещества белковой природы, вырабатываемые клетками живых организмов.
- 35. 5. Катализ Ферменты отличаются рядом свойств от неорганических катализаторов: 1. Высокая каталитическая активность- определяется количеством молекул
- 36. 5. Катализ 2. Высокая скорость ( в 106 – 1012 раз превышает скорости некаталитических реакций). 3.
- 37. 5. Катализ Кинетика ферментативных процессов изучалась Михаэлисом и Ментен (1913 г.) Представим схему ферментативного процесса: Фермент-энзим
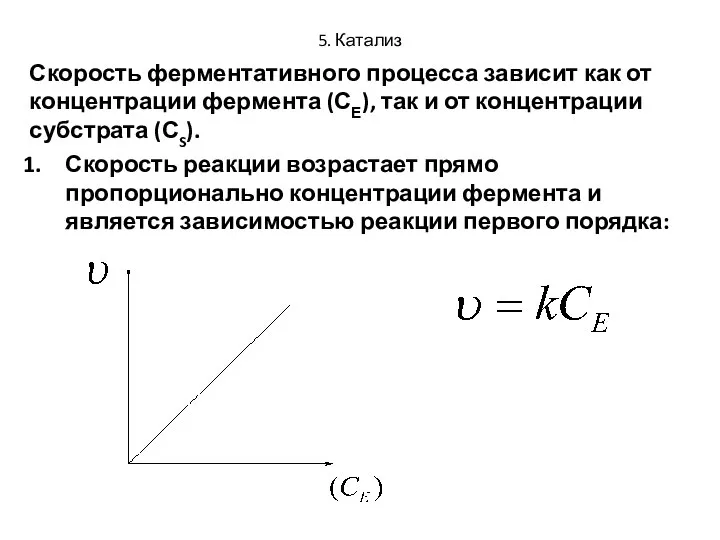
- 38. 5. Катализ Скорость ферментативного процесса зависит как от концентрации фермента (СЕ), так и от концентрации субстрата
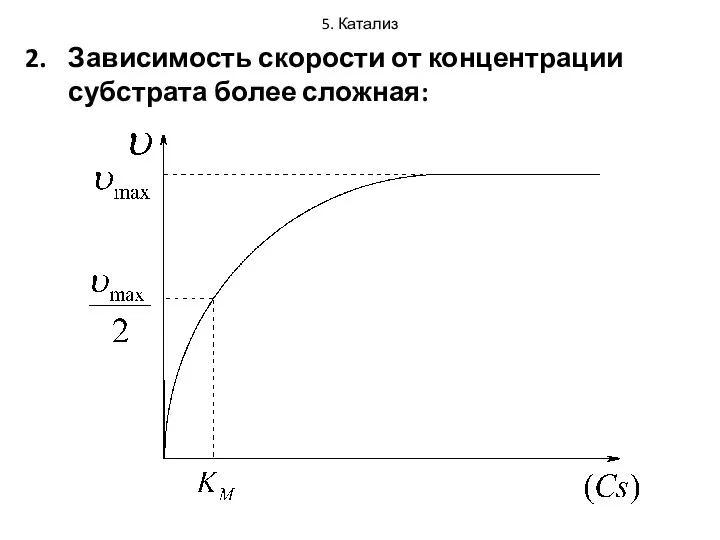
- 39. 5. Катализ Зависимость скорости от концентрации субстрата более сложная:
- 40. 5. Катализ При небольших концентрациях субстрата зависимость соответствует первому порядку реакции: В этом случае все молекулы
- 41. 5. Катализ При дальнейшем увеличении концентрации субстрата наступает момент насыщения активных центров фермента и рост концентрации
- 42. 5. Катализ Математически зависимость скорости от концентрации субстрата выражается кинетическим уравнением Михаэлиса-Ментен (1913 г): , где
- 43. 5. Катализ КМ – константа диссоциации фермент-субстратного комплекса или константа Михаэлиса [моль∙л-1] Величина КМ численно равна
- 44. 5. Катализ В настоящее время известно свыше 2000 ферментов, учение о них выделено в самостоятельную науку
- 45. 6. Действие ингибиторов 1. Защитное действие ингибиторов коррозии определяется их способностью изменять кинетику электрохимических реакций, обусловливающих
- 46. 6. Действие ингибиторов 2. Антиоксиданты. Ингибиторы окисления пищевых продуктов — природные или синтетические вещества, задерживающие окисление
- 47. 6. Действие ингибиторов Синтетические антиоксиданты (так называемые присадки) применяются для предохранения от окисления нефтепродуктов, смазочных масел,
- 48. 6. Действие ингибиторов 1. Ингибиторы, обрывающие цепи по реакции с пероксильными радикалами. Такими ингибиторами являются ароматические
- 49. 6. Действие ингибиторов 1. Ингибиторы, обрывающие цепи по реакции с пероксильными радикалами. Такими ингибиторами являются ароматические
- 50. 6. Действие ингибиторов 6. Ингибиторы комбинированного действия. Некоторые соединения тормозят окисление, одновременно вступая в несколько реакций.
- 51. 6. Действие ингибиторов 3. Лекарственные вещества – ингибиторы (блокаторы). Механизм биологического действия некоторых фарм. препаратов заключается
- 53. Скачать презентацию















































 Йод, химия, 9 класс
Йод, химия, 9 класс Презентация по Химии "Щелочные металлы" - скачать смотреть
Презентация по Химии "Щелочные металлы" - скачать смотреть  Кристаллохимия. Тығыз шарлар теориясы
Кристаллохимия. Тығыз шарлар теориясы Карбоновые кислоты и их производные
Карбоновые кислоты и их производные Металдар. металдардың периодтық жүйедегі орны. Металдардың құрылысы
Металдар. металдардың периодтық жүйедегі орны. Металдардың құрылысы Группа веществ, изолируемых из биологического материала экстракцией и сорбцией. (Лекция 6)
Группа веществ, изолируемых из биологического материала экстракцией и сорбцией. (Лекция 6) Алкины. Общая характеристика, гомологический ряд, номенклатура, изомерия. Методы синтеза алкенов. Лекция №4
Алкины. Общая характеристика, гомологический ряд, номенклатура, изомерия. Методы синтеза алкенов. Лекция №4 Производные ненасыщенных полиокси-γ-лактонов
Производные ненасыщенных полиокси-γ-лактонов Кобальт. Нахождение Co в природе
Кобальт. Нахождение Co в природе Презентация по Химии "Моделирование. Геометрия молекул." - скачать смотреть бесплатно
Презентация по Химии "Моделирование. Геометрия молекул." - скачать смотреть бесплатно Презентация по Химии "Комплексные соединения: строение, изомерия, использование в онкологии" - скачать смотреть
Презентация по Химии "Комплексные соединения: строение, изомерия, использование в онкологии" - скачать смотреть  Алкадиены. Строение, изомерия, номенклатура, физические и химические свойства
Алкадиены. Строение, изомерия, номенклатура, физические и химические свойства Гетероциклдік қосылыстар
Гетероциклдік қосылыстар Загрязнение продуктов питания примесями, мигрирующими из оборудования, инвентаря, тары и упаковочных материалов
Загрязнение продуктов питания примесями, мигрирующими из оборудования, инвентаря, тары и упаковочных материалов Экспериментальное исследование кипения сверхтекучего гелия на цилиндрическом нагревателе внутри пористой оболочки
Экспериментальное исследование кипения сверхтекучего гелия на цилиндрическом нагревателе внутри пористой оболочки Найважливіші мікробіологічні процеси, збудники яких є мікроорганізми
Найважливіші мікробіологічні процеси, збудники яких є мікроорганізми Галогены. Физические свойства галогенов
Галогены. Физические свойства галогенов Металлы: общая характеристика
Металлы: общая характеристика Аналитические химические реакции. Классификация аналитических химических реакций
Аналитические химические реакции. Классификация аналитических химических реакций Brain элементтері
Brain элементтері Углеводороды. Обобщение знаний
Углеводороды. Обобщение знаний Материалы с особыми технологическими свойствами
Материалы с особыми технологическими свойствами Обмен липидов-2
Обмен липидов-2 Алкілування ізобутану бутенами
Алкілування ізобутану бутенами Неорганические соединения азота
Неорганические соединения азота Ферменты. Уравнение Михаэлиса-Ментен
Ферменты. Уравнение Михаэлиса-Ментен Обмен липидов
Обмен липидов Пористые адсорбенты. Лекция 06
Пористые адсорбенты. Лекция 06