Анализ ошибок. Управление рисками причинения вреда здоровью пациентов при оказании медицинской помощи
Содержание
- 2. Риск-менеджмент Управление рисками причинения вреда здоровью пациентов при оказании медицинской помощи (риск-менеджмент) является одним из наиболее
- 3. Статистика причинения вреда здоровью Исследователи (США, Канада, Великобритания, Австралия) установили, что какой-либо вред здоровью, обусловленный не
- 4. США ежегодно порядка 2,1 млн. людей становятся жертвами ошибки врача, а экономический ущерб оценивается ≈ 29
- 5. Статистика врачебных ошибок Отчёт института медицины США (1999 год): от 44 до 98 тысяч человек погибают
- 6. Сколько умирает у нас ? Какие потери при этом несет наша страна? В Казахстане не принято
- 7. Комитет контроля медицинской и фармацевтической деятельности Как правило, оперирует количеством принятых жалоб и показателем их обоснованности.
- 8. По мнению Lucian Leape из Harvard School of Public Health проблема не в некомпетентности: "Плохие врачи
- 10. Термины и определения Основными понятиями в терминологии ВОЗ по безопасности пациентов являются «неблагоприятное событие» («adverse event»)
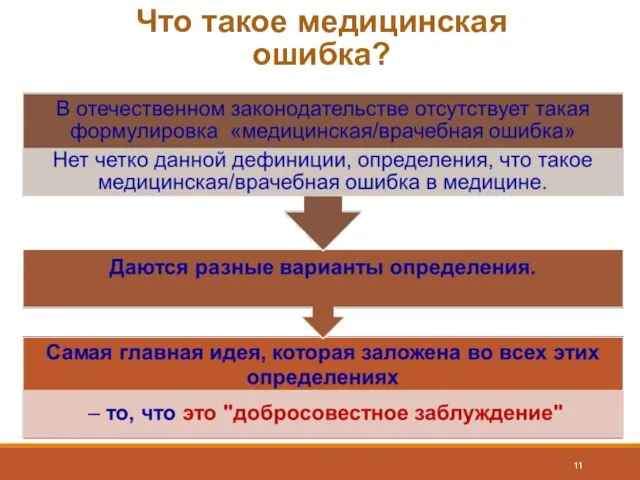
- 11. Что такое медицинская ошибка?
- 12. Медицинские ошибки Медицинские ошибки – невыполнение запланированного плана действий или следование неверному плану в достижении поставленной
- 13. Обеспечение безопасности пациентов Согласно концепции ВОЗ, обеспечение безопасности пациентов должно проводиться по нескольким направлениям: 1) профилактика
- 14. Методы выявления и оценки ошибок и неблагоприятных событий Ретроспективный анализ медицинской документации Проведение опросов (интервьюирование) медицинского
- 15. 1. Ретроспективный анализ медицинской документации Медицинская документация – ценный источник информации о характере и распространенности неблагоприятных
- 16. 1. Ретроспективный анализ медицинской документации Недостатки: Невозможность проведения глубокого анализа конкретных, единичных неблагоприятных событий (в мед.картах
- 17. 2. Проведение опросов медицинского персонала и пациентов в выявлении в выяснении причин Высокая эффективность: Преимущества: Возможность
- 18. 3. Непосредственное наблюдение за процессом оказания медицинской помощи Преимущества: Высокая эффективность Может осуществляться в режиме реального
- 19. 4. Отчетность сотрудников организаций здравоохранения об ошибках и неблагоприятных событиях Цель – получить информацию не только
- 20. 5. Анализ жалоб и судебных исков пациентов Не каждое НС может приводить к возникновению жалобы или
- 21. 6. Компьютерный мониторинг электронных баз медицинских организаций Обеспечение безопасности медикаментозного лечения (правильность назначений, отпуска, приема лекарств)
- 22. 7. Патологоанатомические исследования Проводится с целью определения причин смерти, уточнения или изменения диагноза, выставленного при жизни
- 23. 8. Клинико-анатомические конференции Основное преимущество – обучающий компонент: Экспресс-анализ ситуации, позволяющий сделать определенные выводы и на
- 24. Выбор метода исследования Сравнительный анализ методов не позволяет выделить какой-либо универсальный, подходящий для решения всех вопросов,
- 25. Ошибки и обман при проведении клинических исследований «В мире нет ничего неизбежного, за исключением смерти и
- 26. Мониторинг – деятельность, заключающаяся в контроле за ходом клинического исследования, обеспечении его проведения, сбора данных и
- 27. Цели мониторирования Убедиться что: права и благополучие субъектов защищены представленные данные являются точными, полными и подтверждаются
- 28. Обязанности монитора проверить адекватность квалификации исследователей и достаточность имеющегося персонала для проведения исследований проверка соблюдения исследователем
- 29. Обязанности монитора проверить правильность и полноту данных в ИРК, первичных документах и других относящихся к исследованию
- 30. Контроль качества главный исследователь, исследовательская команда монитор центра (мониторинговый визит) спонсор / КИО (ко-мониторинговый визит) Data
- 31. Аудит – систематический и независимый контроль, связанный с проведением исследования процедур и документов с целью убедиться,
- 32. Цели и задачи аудита Убедиться что: обеспечивается безопасность и соблюдаются права субъектов исследования исследователь и персонал
- 33. Виды аудитов Внутренний – проводится сотрудниками отдела качества фармацевтической компании или КИО, которые непосредственно участвуют в
- 34. Кем проводится? Аудит осуществляется тем персоналом, который «...независим, не связан с выполнением текущего мониторинга и контроля
- 35. Объекты проверки Случайно выбранные исследования 100% информированные согласия 100% несовершеннолетних пациентов 100% серьезные нежелательные явления Регуляторные
- 36. Инспекция – действие уполномоченных органов, заключающееся в официальной проверке документации, оборудования, иных материалов, имеющих, по мнению
- 37. FDA инспекция Плановые – центры для проведения плановых инспекций выбираются наугад, когда нет подозрений в каких-либо
- 38. Объекты инспекции Роль каждого участника исследования, входящего в группу исследователя Степень делегирования полномочий от исследователя. Где
- 39. Обман (falsification) - представление как неправильной информации (например, ложные данные), так и наоборот, несообщение важной информации
- 40. Нарушения в проведении исследования (misconduct) – несоответствие стандартам проведения клинического исследования. Нарушения в проведении исследования могут
- 41. Подлог (fraud) - внесение преднамеренных изменений незначительное количество данных, приводящее к полной фальсификации целого исследования. Так,
- 42. 1. Измененные данные - получение неточных или изменение данных, которые были получены соответствующим образом, например раскрытие
- 43. Ошибки описания статистических методов Кроме ошибок, являющихся результатом неправомерного использования тех или иных статистических методов, немалое
- 44. Качество публикаций Анализ более 1500 опубликованных статей и диссертаций биомедицинской тематики, проведенный некоторыми исследователями, в течение
- 45. Почему важна конкретизация в тексте всей схемы статистического анализа экспериментальных данных, включая указание использованных при этом
- 46. Оставшиеся 75% работ содержат в той или иной форме описание использованных методов статистики, обычно в разделе
- 47. Описание использованных методов статистики 2) Для второй группы работ (примерно 30%) характерно указание на более конкретные
- 48. Описание использованных методов статистики 3) Третья группа проанализированных работ (примерно 25%) содержит достаточно безграмотные, а подчас
- 49. Классификация результатов NAI — no action indicated. Требования к проведению исследования соблюдены полностью; VAI — voluntary
- 50. Дисквалификация исследователей В том случае, если в ходе инспекции будет выявлено, что исследователь неоднократно или намеренно
- 51. Дисквалификация исследователей
- 52. FDA инспекция В течение 15 дней в FDA должен быть послан ответ с планом корректирующих мероприятий
- 54. Скачать презентацию

















































 Иммунитет. Цитокиновая система
Иммунитет. Цитокиновая система Синдром фето-фетальной трансфузии
Синдром фето-фетальной трансфузии Рак яичников при эндометриозе
Рак яичников при эндометриозе Совет по сестринскому делу
Совет по сестринскому делу Соблюдения требований санитарного законодательства при организации отдыха и оздоровления детей
Соблюдения требований санитарного законодательства при организации отдыха и оздоровления детей Диспансерное наблюдение детей с бронхиальной астмой
Диспансерное наблюдение детей с бронхиальной астмой Лабораторный процесс и практическое обучение медицинского лабораторного техника
Лабораторный процесс и практическое обучение медицинского лабораторного техника Моральное и эмоциональное развитие детей
Моральное и эмоциональное развитие детей Шизофрения. Эпилепсия. Маниакально-депрессивный психоз. Бредовые идеи. Расстройства памяти и интеллекта
Шизофрения. Эпилепсия. Маниакально-депрессивный психоз. Бредовые идеи. Расстройства памяти и интеллекта Профилактика простудных и вирусных заболеваний
Профилактика простудных и вирусных заболеваний Общий уход за больными, как дисциплина
Общий уход за больными, как дисциплина Упражнения для достижения цели
Упражнения для достижения цели Семиотика поражений костной системы у детей
Семиотика поражений костной системы у детей Язвенная болезнь и меры профилактики
Язвенная болезнь и меры профилактики Аутистические расстройства в детском возрасте: проблема диагностических критериев
Аутистические расстройства в детском возрасте: проблема диагностических критериев Воспалительные заболевания придатков матки: диагностика и лечение
Воспалительные заболевания придатков матки: диагностика и лечение Нормы питания
Нормы питания Формирование мотивационного компонента готовности к обучению в школе через развитие познавательных процессов дошкольников
Формирование мотивационного компонента готовности к обучению в школе через развитие познавательных процессов дошкольников Цвет в поэзии как отражение психологического состояния автора. Сергей Александрович Есенин 1895-1925 гг
Цвет в поэзии как отражение психологического состояния автора. Сергей Александрович Есенин 1895-1925 гг 1SanProsvet
1SanProsvet Санаторий–профилакторий Энергетик
Санаторий–профилакторий Энергетик Профилактика инфекционных заболеваний у детей
Профилактика инфекционных заболеваний у детей Острая сенсоневральная тугоухость
Острая сенсоневральная тугоухость Протокол лечения пациентов с анафилактическим шоком
Протокол лечения пациентов с анафилактическим шоком Ультразвуковая диагностика селезенки. (Лекция 3)
Ультразвуковая диагностика селезенки. (Лекция 3) Нематоды 1. Общая и медицинская гельминтология. Лекция 06
Нематоды 1. Общая и медицинская гельминтология. Лекция 06 «Дом для мамы»: я выбираю жизнь
«Дом для мамы»: я выбираю жизнь Интубация трахеи
Интубация трахеи