Содержание
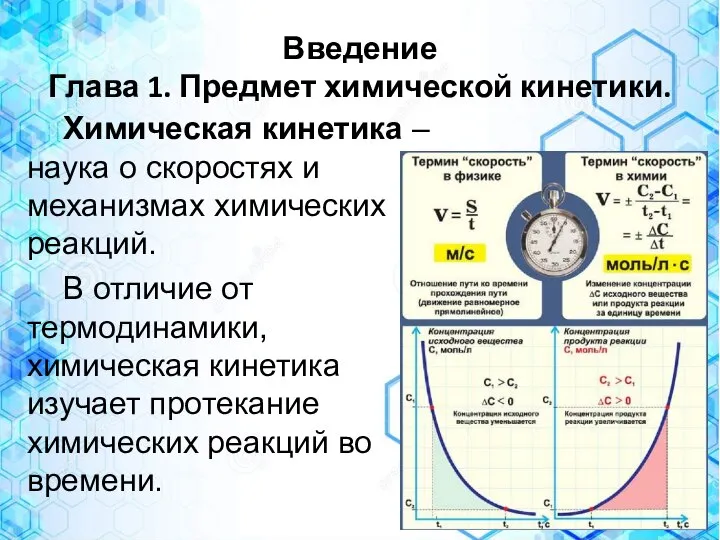
- 2. Введение Глава 1. Предмет химической кинетики. Химическая кинетика – наука о скоростях и механизмах химических реакций.
- 3. 1.2 Основные понятия химической кинетики Механизм химической реакции – это совокупность стадий, из которых она складывается.
- 4. Механизм реакции: (0) H2 + O2 → 2 OH •– зарождение цепи. Это – разветвленный цепной
- 5. 2. Простые и сложные реакции. Простыми называются реакции, состоящие только из одной стадии. Сложными называются реакции,
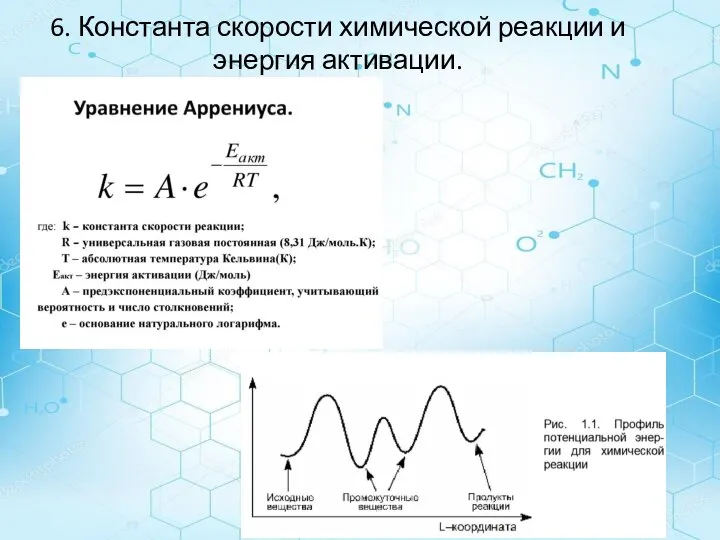
- 6. 6. Константа скорости химической реакции и энергия активации.
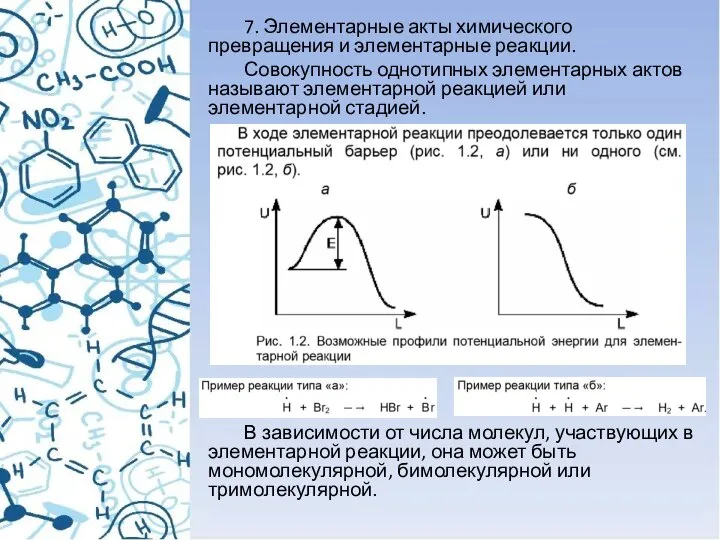
- 7. 7. Элементарные акты химического превращения и элементарные реакции. Совокупность однотипных элементарных актов называют элементарной реакцией или
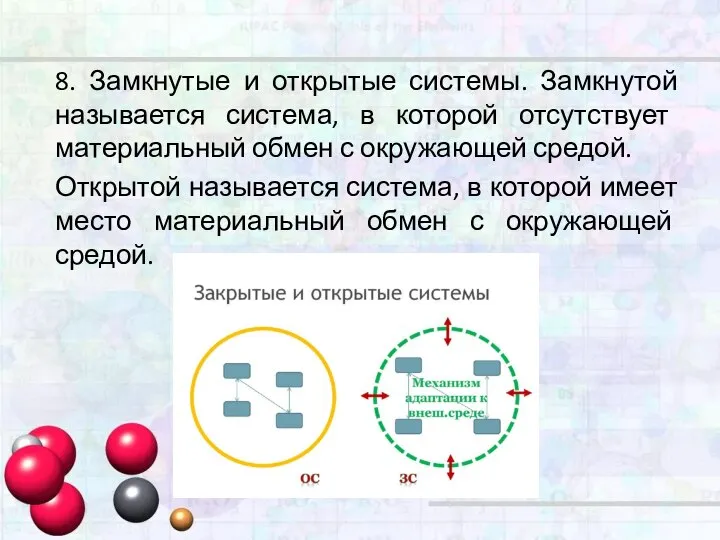
- 8. 8. Замкнутые и открытые системы. Замкнутой называется система, в которой отсутствует материальный обмен с окружающей средой.
- 9. Глава 2. Формальная кинетика простых реакций 2.1 Закон действующих масс Формальная кинетика – это раздел кинетики,
- 10. Скорость химической реакции определяется как изменение молярной концентрации одного из реагирующих веществ за единицу времени.
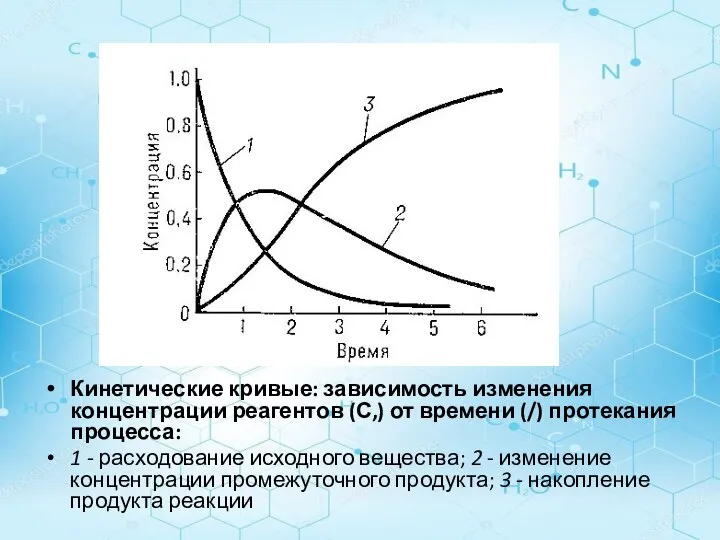
- 13. Кинетические кривые: зависимость изменения концентрации реагентов (С,) от времени (/) протекания процесса: 1 - расходование исходного
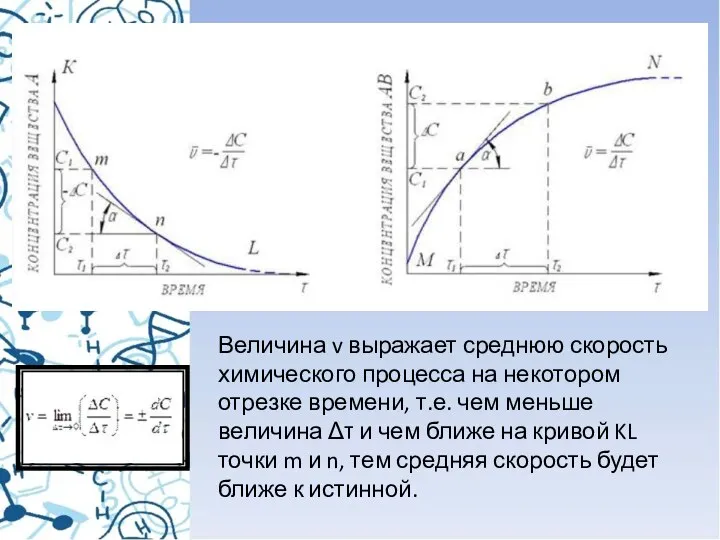
- 14. Величина v выражает среднюю скорость химического процесса на некотором отрезке времени, т.е. чем меньше величина Δτ
- 15. Молекулы, обладающие такой избыточной энергией, называются активными, а сам избыток энергии - энергией активации(Еа). Понятно, что,
- 16. Важнейшие пути активации: 1) Увеличение кинетической энергии молекулы (например, путем повышения температуры системы); 2) Повышение внутримолекулярной
- 17. Зависимость скорости реакции от реагирующий веществ Чем больше концентрация реагирующих веществ, тем больше столкновений и, соответственно,
- 18. Реакции первого порядка. В реакциях первого порядка скорость пропорциональна концентрации одного реагирующего вещества. Выражение скорости, как
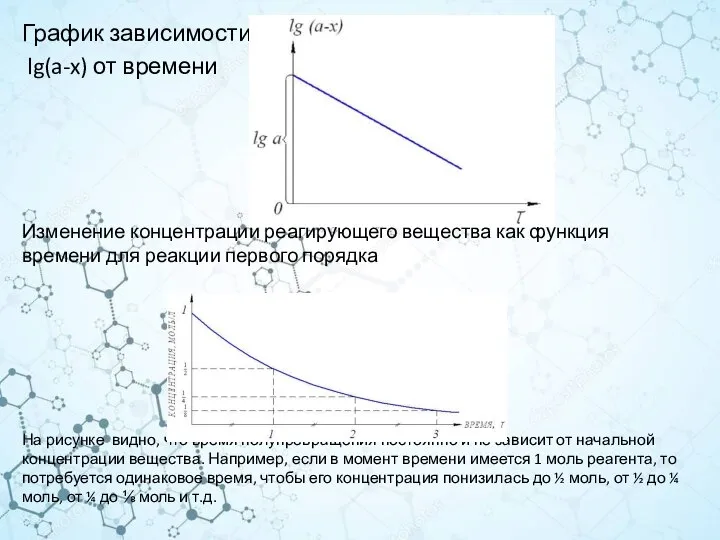
- 19. График зависимости lg(a-x) от времени Изменение концентрации реагирующего вещества как функция времени для реакции первого порядка
- 20. Реакции второго порядка. В общем виде уравнение реакции второго порядка можно записать следующим образом: A +
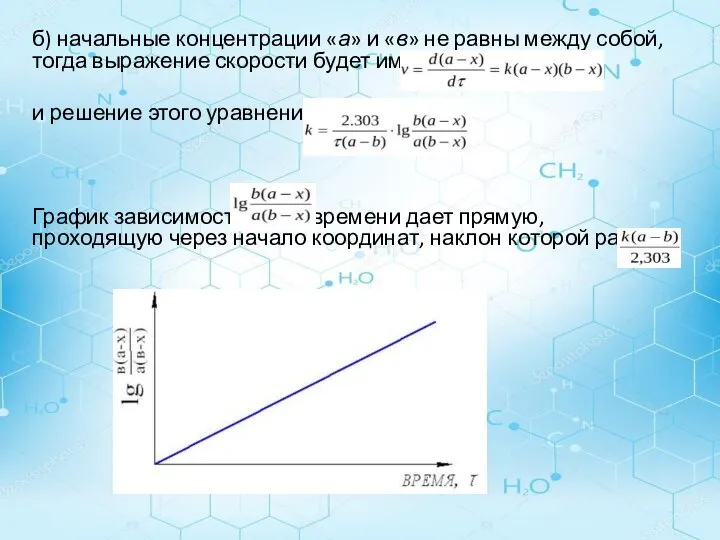
- 21. б) начальные концентрации «а» и «в» не равны между собой, тогда выражение скорости будет иметь вид:
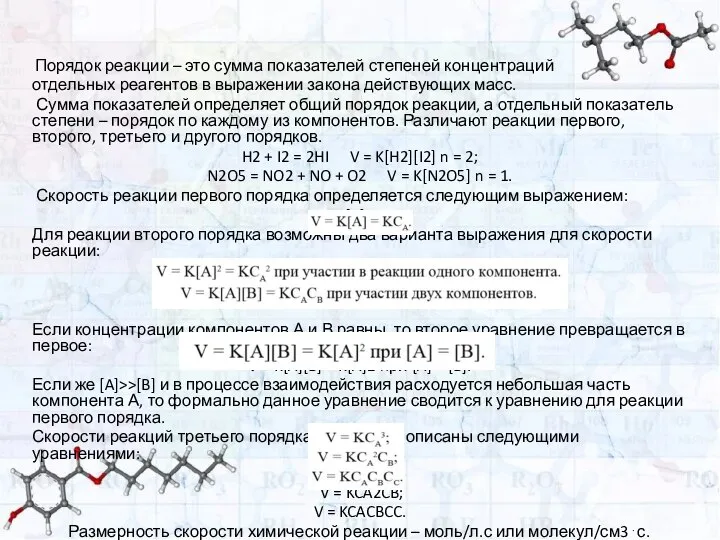
- 22. Порядок реакции – это сумма показателей степеней концентраций отдельных реагентов в выражении закона действующих масс. Сумма
- 23. По механизму реакции можно разделить на 6 типов: а) последовательные реакции: A → B → C.
- 24. б) параллельные реакции: B ← A → C Параллельными называются реакции, имеющие одни и те же
- 25. в) сопряженные реакции (одна реакция идет в присутствии другой). Примером такого процесса являются следующие реакции: 1.
- 26. г) цепные реакции. Цепные реакции распространены в химии. Эти реакции вызываются свободными радикалами, активными частицами, образовавшимися
- 27. Обрыв цепи – стадия реакции, в результате которой исчезают свободные радикалы. Общая скорость неразветвлённой цепной реакции
- 28. д) периодические реакции (автоколебательные реакции). Эти реакции открыты Б.П. Белоусовым, исследованы А.М. Жаботинским и др. (СССР).
- 30. Скачать презентацию


















 Введение в химическую термодинамику
Введение в химическую термодинамику Посвящение в химики!
Посвящение в химики! Ионно-координационная полимеризация
Ионно-координационная полимеризация Презентация по Химии "Химия. Щелочные металлы" - скачать смотреть
Презентация по Химии "Химия. Щелочные металлы" - скачать смотреть  Робота учня 11-В класу: Андрійка Андрія
Робота учня 11-В класу: Андрійка Андрія  Д. И. Менделеев человек - загадка Автор: Ким Н. В. учитель химии 2008 год.
Д. И. Менделеев человек - загадка Автор: Ким Н. В. учитель химии 2008 год.  Физическая химия. Химическая термодинамика
Физическая химия. Химическая термодинамика Крахмал (C6H10O5)n
Крахмал (C6H10O5)n  Сера и ее соединения
Сера и ее соединения Текстуры метаморфических пород
Текстуры метаморфических пород Итоговая консультация. Формульный диктант
Итоговая консультация. Формульный диктант Химическая связь
Химическая связь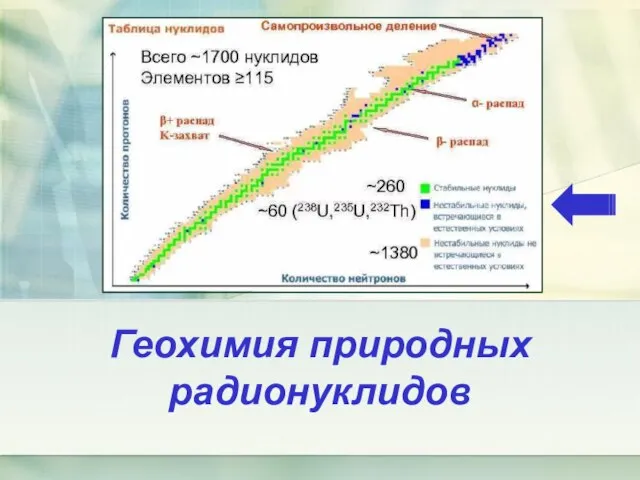 Геохимия природных радионуклидов (тема 1)
Геохимия природных радионуклидов (тема 1) Медь. Содержание в природе
Медь. Содержание в природе Щелочи
Щелочи Теория химического строения органических соединений А.М. Бутлерова (ТХС)
Теория химического строения органических соединений А.М. Бутлерова (ТХС) Химический элемент таблицы Менделеева - Азот
Химический элемент таблицы Менделеева - Азот Химические реакции органических соединений
Химические реакции органических соединений Производство метанола и этанола
Производство метанола и этанола Хром (Cr)
Хром (Cr) Строение, свойства и функции аминокислот и белков
Строение, свойства и функции аминокислот и белков Презентация по Химии "Химическая связь" - скачать смотреть бесплатно
Презентация по Химии "Химическая связь" - скачать смотреть бесплатно Второй закон термодинамики
Второй закон термодинамики Кинетика химических реакций
Кинетика химических реакций Топливо и топливосжигающие устройства. Горение топлива
Топливо и топливосжигающие устройства. Горение топлива Оцет Яковлев Олексій 11-В
Оцет Яковлев Олексій 11-В  Липиды. Классификация липидов
Липиды. Классификация липидов Химические свойства карбокатионов
Химические свойства карбокатионов