Железо Железо не только основа всего мира, самый главный металл окружающей нас природы, оно – основа культуры и промышленности,
Содержание
- 2. Строение атома железа. Задание: прочитайте текст учебника стр. 76 и охарактеризует положение химического элемента железа в
- 3. Нахождение в природе. Халькопирит с включениями кварца Приморский край Пирит
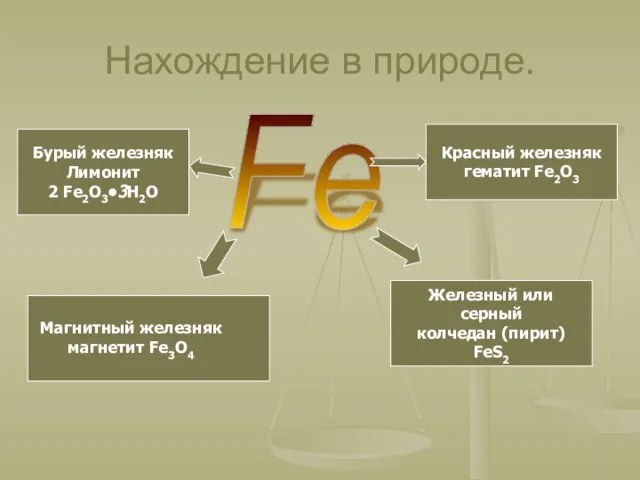
- 4. Нахождение в природе. Fe Магнитный железняк магнетит Fe3O4 Красный железняк гематит Fe2O3 Бурый железняк Лимонит 2
- 5. Физические свойства Железо - сравнительно мягкий ковкий серебристо-серый металл. Температура плавления – 1535 0С Температура кипения
- 6. Химические свойства железа 1. Железо реагирует с неметаллами: Fe + S = FeS При нагревании до
- 7. Химические свойства железа 2. Железо реагирует с кислотами. Fe+H2SO4=FeSO4+H2 В концентрированных азотной и серной кислотах железо
- 8. Химические свойства железа. 3. Реагирует с растворами солей металла согласно электрохимическому ряду напряжений металлов. Fe +
- 9. Химические свойства Прочитайте текст учебника, составьте уравнения реакций Fe+H2О Fe+CuSO4 Fe+O2 Сделайте вывод о химической активности
- 10. Биологическая роль железа Железо играет важную роль в жизнедеятельности живых организмов. Оно входит в состав гемоглобина
- 12. Скачать презентацию








 Знаки химических элементов. Тренажер
Знаки химических элементов. Тренажер Презентация по Химии "КАРБОНОВЫЕ КИСЛОТЫ" - скачать смотреть
Презентация по Химии "КАРБОНОВЫЕ КИСЛОТЫ" - скачать смотреть  Синтетикалық полимерлер (пластиктер)
Синтетикалық полимерлер (пластиктер) Основные законы химии
Основные законы химии Применение дидактических игр на уроках химии
Применение дидактических игр на уроках химии Состав вещества
Состав вещества Металлы II А группы
Металлы II А группы Липидтер
Липидтер Защитные материалы
Защитные материалы Кислород. Получение кислорода и его физические свойства урок-презентация по химии 8 класс учитель: Видершпан И.П.
Кислород. Получение кислорода и его физические свойства урок-презентация по химии 8 класс учитель: Видершпан И.П. Углерод. Металлы. 9 класс
Углерод. Металлы. 9 класс МОЮЩИЕ СРЕДСТВА СВОЙСТВА МОЮЩИХ СРЕДСТВ КЛАССИФИКАЦИЯ МОЮЩИХ СРЕДСТВ
МОЮЩИЕ СРЕДСТВА СВОЙСТВА МОЮЩИХ СРЕДСТВ КЛАССИФИКАЦИЯ МОЮЩИХ СРЕДСТВ Кислоты. Химические свойства
Кислоты. Химические свойства Белки плазмы крови, их биологическая роль. Методы разделения белков плазмы крови. Диспротеинемии. Выполнила студентка 6 курса МБФ
Белки плазмы крови, их биологическая роль. Методы разделения белков плазмы крови. Диспротеинемии. Выполнила студентка 6 курса МБФ Аттестационная работа. Исследовательская работа. Влияет ли зубная паста на прочность зубов
Аттестационная работа. Исследовательская работа. Влияет ли зубная паста на прочность зубов Органические вещества спирты
Органические вещества спирты Химические свойства солей и их применение
Химические свойства солей и их применение Обмен липидов
Обмен липидов Как вести себя при встрече с агрессивными собаками Как вести себя при встрече с агрессивными собаками
Как вести себя при встрече с агрессивными собаками Как вести себя при встрече с агрессивными собаками Ароматичні вуглеводні Арени Підготував Учень 11-А класу Пазуханич Руслан
Ароматичні вуглеводні Арени Підготував Учень 11-А класу Пазуханич Руслан  История развития химии
История развития химии Висмут Bi
Висмут Bi Сера. Нахождение в природе. Химические свойства серы
Сера. Нахождение в природе. Химические свойства серы Керамические материалы и изделия
Керамические материалы и изделия Обмен липидов. Часть 2
Обмен липидов. Часть 2 Презентация по Химии "ХИМИЯ НА КУХНЕ" - скачать смотреть бесплатно
Презентация по Химии "ХИМИЯ НА КУХНЕ" - скачать смотреть бесплатно Получение металлов
Получение металлов Пәнге кіріспе. Жалпы технологиялық түсініктер мен терминдер. Өнеркәсіптік регламент негізгі нормативті-техникалық құжат ретінде
Пәнге кіріспе. Жалпы технологиялық түсініктер мен терминдер. Өнеркәсіптік регламент негізгі нормативті-техникалық құжат ретінде